双分子亲核取代反应

SN2反应(双分子亲核取代反应)是亲核取代反应的一类,其中S代表取代(Substitution),N代表亲核(Nucleophilic),2代表反应的决速步涉及两种分子。与SN1反应相对应,SN2反应中,亲核试剂带着一对孤对电子进攻具亲电性的缺电子中心原子,形成过渡态的同时,离去基团离去。反应中不生成碳正离子,速率控制步骤是上述的协同步骤,反应速率与两种物质的浓度成正比,因此称为双分子亲核取代反应。
在无机化学中,常称双分子亲核取代反应类型的反应机理为“交换机理”。
反应机理
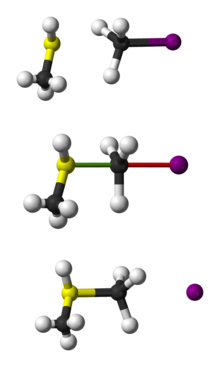
[编辑]SN2反应最常发生在脂肪族sp3杂化的碳原子上,碳原子与一个电负性强、稳定的离去基团(X)相连,一般为卤素阴离子。亲核试剂(Nu)从离去基团的正后方进攻碳原子,Nu-C-X角度为180°,以使其孤对电子与C-X键的σ*反键轨道可以达到最大重叠。然后形成一个五配位的反应过渡态,碳约为sp2杂化,用两个垂直于平面的p轨道分别与离去基团和亲核试剂成键。C-X的断裂与新的C-Nu键的形成是同时的,X很快离去,形成含C-Nu键的新化合物。
由于亲核试剂是从离去基团的背面进攻,故如果受进攻的原子具有手性,则反应后手性原子的立体化学发生构型翻转,也称“瓦尔登翻转”。这也是SN2反应在立体化学上的重要特征。反应过程类似于大风将雨伞由里向外翻转。

上例中,OH−(亲核试剂)进攻C2H5Br(底物)发生SN2反应,经过不稳定的过渡态,最终Br−离去,得到乙醇。
SN2反应也可以在分子内发生,合成的环系一般为五元环、六元环和三元环。分子内的Williamson合成得到环氧化合物,即是这类反应的一个例子。相比下,四元环张力太大,空间上也不利,很难生成;七元、八元之类的大环可以生成,但分子间反应处于优势,需要将反应物以高稀溶液的形式反应,以增大分子内产物的比例。
SN2反应一般发生在伯碳原子上,很难成为有位阻分子的反应机理,并且取代基越多,按SN2机理反应的可能性越小。基团在空间上比较拥挤的分子一般采用SN1机理,可以缓解一部分的位阻,也可生成较稳定的碳正离子(通常为三级碳正离子)。
决定速率的因素
[编辑]- 离去基团的碱性:离去基团的碱性越强,其离去能力越弱,反之亦然。离子的碱性随着所在周期的增加而降低。对于卤素离子而言,碘离子的碱性最弱,因此碘离子是一个很好的离去基团;氟离子则相反,氟代烃也因此很难发生SN2反应。
- 强碱 F− > Cl− > Br− > I− 弱碱
- 反应速率 慢 F− < Cl− < Br− < I− 快
- 亲核试剂的亲核性:亲核性需要与上面的碱性相区别。碱性是试剂对质子的亲和能力,而亲核性是试剂形成过渡态时,对碳原子的亲和能力。一般来讲,试剂的电负性、碱性和可极化性越强,其亲核性也越强,因此反应越快。实际上通常需要综合考虑这几个因素以及溶剂的影响。
- 溶剂:SN2反应在质子溶剂中进行时,一方面,溶剂化作用有利于离去基团的离去;另一方面,溶剂也会与亲核试剂发生作用,使亲核试剂与底物的接触变得困难。最后的影响是这两种因素的综合结果。相对而言,極性非質子性分子很少包围负离子,因此对SN2反应是有利的。
- 空间效应:立體阻礙性(含体积大的取代基)会使亲核试剂的亲核性下降从而导致反应变慢。虽然乙醇的酸性比叔丁醇强,但叔丁氧基负离子的亲核性弱于乙氧基负离子,就是因为这个缘故。
- 空間效應:分子大小。分子越大,位阻增加,減慢反應。叔碳分子基本上沒可能發生反應。反應速度:(快)伯>仲>叔(慢)
反应动力学
[编辑]SN2属于二级反应,决速步与两个反应物的浓度相关:亲核试剂[Nu−]和底物[RX]。
- r = k[RX][Nu−]
与此相对比的是单分子亲核取代反应—SN1反应,亲核取代反应的另一种机理。此类反应中,底物中的C-X键首先异裂为碳正离子和X−,是较慢的一步,然后亲核试剂Nu−立即与碳正离子结合,得到含C-Nu键的产物。因此该反应的速率控制步骤只和底物的浓度有关,称为单分子亲核取代反应。
需要注意的是,SN1和SN2只是亲核取代反应的两个比较极端的机理,属于理想情况。在因素如离子对的影响下,实际中的反应都会或多或少地兼具这两者机理的成分,有些甚至难以归类。至于反应按哪种机理进行的成分多一些,与具体的反应物结构、类型、溶剂、浓度、温度、亲核试剂、离去基团等因素都有很密切的关系。
E2竞争
[编辑]双分子亲核取代反应的一个副反应是E2消除反应:亲核试剂表现碱性,从底物的β-碳夺取氢离子,底物发生消除反应生成烯烃。SN2反应与E2反应的共存与竞争可通过以下实验体现:[1]
上述是磺酸盐负离子与溴代烷在气相发生反应的结果。在水溶液中的趋势是类似的,但还要考虑溶剂效应的影响。当反应物由溴乙烷变为异丁基溴时,位阻大大增加,因此产物也主要变为消除产物。此外,试剂的碱性越强,也会使消除反应产物比例增大。若以碱性更弱的苯甲酸根离子与异丁基溴进行上述反应,取代产物为55%,远远高于磺酸盐负离子反应的15%。
另一种机理
[编辑]2008年时有人提出了SN2的另一种机理:“迂回机理”(Roundabout mechanism)。化学家在借助于“交叉分子束成像法”观测氯离子和碘甲烷在气相的反应时发现,当打出的氯离子具有足够的速度时,反应后碘离子的能量总比预期的要少。根据理论分析推测,能量之所以有损失,是因为氯离子与甲基发生碰撞后,甲基围绕碘原子需要进行迂回的转动,之后才有碘离子的离去以及氯甲烷的生成。[2][3][4]
参见
[编辑]参考资料
[编辑]- ^ Gas Phase Studies of the Competition between Substitution and Elimination Reactions Scott Gronert Acc. Chem. Res.; 2003; 36(11) pp 848 - 857; (Article) doi:10.1021/ar020042n
- ^ Imaging Nucleophilic Substitution Dynamics J. Mikosch, S. Trippel, C. Eichhorn, R. Otto, U. Lourderaj, J. X. Zhang, W. L. Hase, M. Weidemüller, and R. Wester Science 11 January 2008 319: 183-186 doi: 10.1126/science.1150238 (in Reports)
- ^ PERSPECTIVES CHEMISTRY: Not So Simple John I. Brauman (11 January 2008) Science 319 (5860), 168. doi:10.1126/science.1152387
- ^ Surprise From SN2 Snapshots Ion velocity measurements unveil additional unforeseen mechanism Carmen Drahl Chemical & Engineering News January 14, 2008 Volume 86, Number 2 p. 9 ,含录像。http://pubs.acs.org/cen/news/86/i02/8602notw1.html (页面存档备份,存于互联网档案馆)


