Lysine
| Lysine | |
 L ou S(+)-lysine 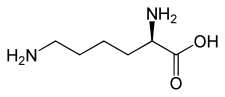 D ou R(–)-lysine |
|
| Identification | |
|---|---|
| Nom UICPA | Acide 2,6-diaminohexanoïque |
| Synonymes |
K, Lys |
| No CAS | (racémique) (L) ou S(+) (D) ou R(–) |
| No ECHA | 100.000.673 |
| No CE | 200-294-2 (L) 213-091-9 (D) |
| Code ATC | B05 |
| FEMA | 3847 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C6H14N2O2 [Isomères] |
| Masse molaire[1] | 146,187 6 ± 0,006 8 g/mol C 49,3 %, H 9,65 %, N 19,16 %, O 21,89 %, |
| pKa | 2,15 / 9,16 / 10,67 |
| Propriétés physiques | |
| T° fusion | 224,5 °C[2] |
| Solubilité | 642 g l−1 d'eau à 20 °C et 780 g l−1 d'eau à 30 °C |
| Thermochimie | |
| Cp | |
| Propriétés biochimiques | |
| Codons | AAA, AAG |
| pH isoélectrique | 9,74[4] |
| Acide aminé essentiel | oui |
| Occurrence chez les vertébrés | 7,2 %[5] |
| Cristallographie | |
| Paramètres de maille | L-lysine : a = 7,492 Å b = 13,320 Å |
| Propriétés optiques | |
| Pouvoir rotatoire | +14,6 |
| Précautions | |
| SIMDUT[7] | |
Produit non contrôlé |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La lysine (abréviations IUPAC-IUBMB : Lys et K) est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, et l'un des neuf acides aminés essentiels pour l'homme. Elle est codée sur les ARN messagers par les codons AAA et AAG[8]. Elle est caractérisée par la présence d'une fonction amine primaire à l'extrémité de sa chaîne latérale, ce qui en fait un résidu basique dans les protéines, tout comme l'arginine et l'histidine.
Poly-L-lysine
[modifier | modifier le code]Le peptide poly-lysine est un polymère de plusieurs lysines. Comme le groupement amine possède un pKa de 10,2, ce groupe est chargé positivement (-NH3+) au pH (neutre) de 7.
Avec ce polymère chargé positivement, l'ADN peut être lié (lors de la construction de micro-arrays[Quoi ?] d'ADN : à pH neutre (et basique), une surface de verre est chargée négativement par les groupes SiO−. Ils peuvent avoir des liaisons électrostatiques avec la polylysine, qui à son tour se lie aux groupes négatifs de phosphate de l'ADN.
Une lame de verre enduite de polylysine aide à fixer une cellule ou un contenu cellulaire à cette plaque, afin de l'observer au microscope à force atomique.
Usages
[modifier | modifier le code]La lysine est un acide aminé essentiel. Elle est donc utilisée en nutrition animale et humaine pour équilibrer les régimes alimentaires. Elle est aussi utilisée chez l'humain comme antiviral pour le traitement de l’herpès et du zona.
Sources diététiques
[modifier | modifier le code]Les bonnes sources de lysine sont des aliments riches en protéines comme les œufs, la viande (en particulier la viande rouge, l'agneau, le porc et la volaille), le soja, les haricots et les pois, le fromage (en particulier le parmesan) et certains poissons (comme le cabillaud et les sardines)[9],[10].
La lysine est l'acide aminé limitant (l'acide aminé essentiel trouvé en plus petite quantité dans un aliment particulier) dans la plupart des céréales, mais est abondante dans la plupart des légumineuses. Un régime alimentaire végétarien ou à faible teneur en protéines animales peut être adéquat pour les protéines, y compris la lysine, si elle comprend à la fois des céréales et des légumineuses, mais il n'est pas nécessaire que les deux groupes d'aliments soient consommés dans les mêmes repas.
Un aliment est considéré comme ayant un taux de lysine suffisant s'il contient au moins 51 mg de lysine par gramme de protéine (de sorte que la proportion est de 5,1 % de lysine). Les aliments contenant des proportions significatives de lysine comprennent :
| Aliment | Lysine (% de protéine) |
|---|---|
| Poisson | 9,19 % |
| Bœuf | 8,31 % |
| Poulet | 8,11 % |
| Lait | 7,48 % |
| Soja | 7,42 % |
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Lysine ».
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-858-6)
- (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary, (consulté le ).
- (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le ).
- « Lysine », sur reciprocalnet.org (consulté le ).
- « Lysine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Donald Voet et Judith G. Voet, Biochimie, Bruxelles, Éditions De Boeck Université, , 2e éd. (ISBN 978-2-8041-4795-2), p. 1290
- (en) PubChem, « Lysine », sur pubchem.ncbi.nlm.nih.gov (consulté le ).
- « Lysine - Complément alimentaire », sur VIDAL (consulté le ).
Voir aussi
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- (en) M.A. Vives, M. Macián, J. Seguer, M.R. Infante et M.P. Vinardell, « Irritancy potential induced by surfactants derived from lysine », Toxicology in Vitro, vol. 11, no 6, décembre 1997, p. 779-783.
Articles connexes
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- (en) Lysine
- Ressources relatives à la santé :
- Notices dans des dictionnaires ou encyclopédies généralistes :





