Chlorure de potassium
| Chlorure de potassium | |

| |
| Identification | |
|---|---|
| Nom UICPA | Chlorure de potassium |
| Synonymes |
Muriate de potassium |
| No CAS | |
| No ECHA | 100.028.374 |
| No CE | 231-211-8 |
| Code ATC | A12, B05 |
| No E | E508 |
| Apparence | cristal incolore, hygroscopique[1], incolore à blanc. |
| Propriétés chimiques | |
| Formule | KCl |
| Masse molaire[3] | 74,551 ± 0,002 g/mol Cl 47,55 %, K 52,45 %, |
| Moment dipolaire | 10,269 ± 0,001 D[2] |
| Propriétés physiques | |
| T° fusion | 770 à 773 °C[1], 790 °C[4] |
| T° ébullition | Point de sublimation : 1 500 °C[réf. souhaitée] |
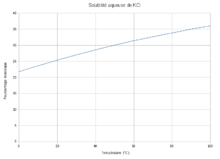
| Solubilité | voir tableau insoluble dans l'acétone |
| Masse volumique | 1,98 g cm−3[1] |
| Thermochimie | |
| ΔfH0liquide | −421,79 kJ mol−1[5] |
| ΔfH0solide | −436,68 kJ mol−1[5] |
| Cp | 51,29 J K−1 mol−1 (solide, 24,85 °C)[5] |
| Cristallographie | |
| Système cristallin | cubique |
| Réseau de Bravais | cF |
| Symbole de Pearson | |
| Classe cristalline ou groupe d’espace | Fm3m, (no 225) |
| Notation Schönflies | |
| Strukturbericht | B1 |
| Structure type | NaCl[6] |
| Propriétés optiques | |
| Indice de réfraction | 1,495 01 1,489 69[réf. souhaitée] |
| Précautions | |
| SIMDUT[7] | |
Produit non contrôlé |
|
| Composés apparentés | |
| Autres cations | Chlorure de lithium Chlorure de sodium Chlorure de rubidium Chlorure de césium |
| Autres anions | Fluorure de potassium Bromure de potassium Iodure de potassium |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le chlorure de potassium est un composé chimique minéral de formule KCl. Sous sa forme solide, ce sel neutre équivaut au minéral tendre[8] nommé sylvine, ou sel amer, ou encore sylvite en anglais, de structure cristallographique cubique à faces centrées[9].
Extraction de la mer
[modifier | modifier le code]Dans les marais salants fortement ensoleillés ou les régions maritimes désertiques, il est possible d'extraire de l'eau de mer le sel amer, soit un chlorure de potassium, plus ou moins associé au chlorure de magnésium, qui apparaît sous forme de saumure et de sels déliquescents, déposés après la halite ou sel marin solide. Dans les pays maritimes dépourvus de ces conditions d'évaporation, l'exploitation moderne des cendres d'algues, en particulier d'algues brunes ou varech, est attestée de manière évidente jusqu'au milieu du XIXe siècle, parfois jusqu'à la Belle Époque car on retirait de la soude de varech brome et iode[10].
-
Femmes amenant au port la soude de varech sur l'île de Sein au début du XXe siècle.
-
Pesage et vérification de la qualité avant l'embarquement sur l'île de Sein pendant l'entre-deux-guerres.
Propriétés chimiques
[modifier | modifier le code]Solubilité
[modifier | modifier le code]Le KCl étant un solide ionique, il est soluble dans de nombreux solvants polaires mais moins dans les solvants apolaires, c'est pourquoi il existe un grand écart de solubilité du chlorure de potassium entre l'eau et l'acétone, par exemple.
| Solvant | Solubilité (g/kg de solvant à 25 °C)[11] |
|---|---|
| Eau | 360 |
| Ammoniac | 0,4 |
| Dioxyde de soufre liquide | 0,41 |
| Méthanol | 5,3 |
| Acide formique | 192 |
| Sulfolane | 0,04 |
| Acétonitrile | 0,024 |
| Acétone | 0,00091 |
| Formamide | 62 |
| Acétamide | 24,5 |
| Diméthylformamide | 0,17–0,5 |
En solution aqueuse, les ions majoritairement formés sont K+ et Cl−.
Propriétés rédox et formation de potassium métallique
[modifier | modifier le code]Bien que le potassium soit plus électropositif que le sodium, KCl peut être réduit à l'état métallique par réaction avec le sodium à 850 °C du fait de la plus grande volatilité du potassium qui peut ainsi être extrait par distillation :
- KCl(l) + Na(l) ⇌ NaCl(l) + K(g).
Cette réaction est la principale méthode de fabrication du potassium métallique. L'électrolyse (utilisée pour le sodium) ne fonctionne pas à cause de la forte solubilité du potassium dans le KCl fondu[12].
Utilisation
[modifier | modifier le code]Alimentation
[modifier | modifier le code]Le chlorure de potassium (numéro E508[13]) est utilisé dans les denrées alimentaires comme remplacement du sel de cuisine (halite, NaCl) car il possède une saveur salée similaire. Cependant, il développe aussi un arrière-goût amer qui permet de les différencier.
Agriculture
[modifier | modifier le code]Le terme générique « potasse » dans la chimie des engrais peut englober le chlorure de potassium ou sylvine, le chlorure double de potassium et de magnésium (nommé sous une forme hydratée carnallite), le sulfate double de potassium et de magnésium, le sulfate de potassium (obtenu par l'action de l'acide sulfurique sur KCl), le nitrate de potassium et l'hydroxyde de potassium KOH, base bien plus forte que l'hydroxyde de sodium NaOH.
Poison
[modifier | modifier le code]La dose létale 50 (dose mesurée sur la souris) de chlorure de potassium est à peu près de 2 500 mg kg−1 par voie orale (c'est-à-dire 190 g pour 75 kg ; à titre de comparaison, le chlorure de sodium (sel de table) a une DL50 orale de 3 750 mg kg−1) et de 100 mg kg−1 en voie intraveineuse. Il est utilisé lors des exécutions de condamnés à mort aux États-Unis, par injection létale : l'administration en intraveineuse d'une solution excessive de KCl provoque un arrêt cardiaque. C’est en raison de cette toxicité qu’en pratique médicale une perfusion de ce soluté ne doit pas dépasser un débit de 1,5 g/h.
Il peut être aussi utilisé pour les interruptions médicales de grossesse par injection intracardiaque fœtale.
Extraction du gaz de schiste par hydrofracturation
[modifier | modifier le code]Le documentaire Gasland (2010) de l'Américain Josh Fox montre que l'industrie américaine de l'extraction du gaz de schiste reconnaît l'usage du chlorure de potassium, dilué dans un mélange d'eau, à d'autres produits chimiques toxiques et de sable pour l'injection dans les puits d'extraction du gaz de schiste comme liquide d'hydrofracturation. Le chlorure de potassium est employé comme absorbeur d'oxygène, mais cette technique visant à libérer le gaz contenu dans la couche de schiste a aussi pour conséquences de polluer les nappes phréatiques avec le liquide de fracturation. Pour un puits d'extraction, il faut entre 10 et 30 000 m3 d'eau, la moitié environ est récupérée après fracturation.
Pharmacochimie
[modifier | modifier le code]Le chlorure de potassium fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[14].
Notes et références
[modifier | modifier le code]- CHLORURE DE POTASSIUM, Fiches internationales de sécurité chimique .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 9-50.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Perry's Chemical Enginner's Handbook[source insuffisante].
- (en) « Potassium chloride », sur NIST/WebBook (consulté le 7 mars 2010).
- (en) Bodie E. Douglas et Shih-Ming Ho, Structure and Chemistry of Crystalline Solids, Pittsburgh, PA, USA, Springer Science + Business Media, Inc., , 346 p. (ISBN 0-387-26147-8), p. 64.
- « Chlorure de potassium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- On peut le rayer à l'ongle.
- Il ne faut le confondre avec la sylvinite, structure isomorphe qui associe intimement NaCl et KCl.
- Le brome et l'iode sont à l'état de traces parfois importantes dans certains goémons ou varechs. La « soude de varech » est une source de potasse pour les Anciens, sous forme KCl ou de sulfate de potassium K2SO4, malheureusement fortement associée au sel marin NaCl. Le nom vient d'une fraction réduite de soude ou Na2CO3, et du fait que les verriers savaient fabriquer de la potasse K2CO3, en séparant le mélange et en chauffant les sels de potasse. Même s'il subsistait des feux libres de goémons à même la plage, il existe aussi de nombreux fours à algues et à soude, installés sur les rivages et les îles, par exemple aux Molènes, aujourd'hui en ruine ou à l'état de traces. La concurrence assez modérée pour le débouché rentable I et Br est venue des nitrates du Chili, puis des mines salines de Stassfurt.
- (en) Burgess, J., Metal Ions in Solution, New York, Ellis Horwood, , 481 p. (ISBN 0-85312-027-7).
- (en) Elizabeth R. Burkhardt, Ullmann's Encyclopedia of Industrial Chemistry, Wiley, (ISBN 978-3-527-30673-2, lire en ligne), « Potassium and Potassium Alloys ».
- (en) Noms de catégorie et système international de numérotation des additifs alimentaires, codex Alimentarius.
- WHO Model List of Essential Medicines, 18th list, avril 2013.
Voir aussi
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- Photo d'un cristal, sur euromin.w3sites.net.










