Alquilo
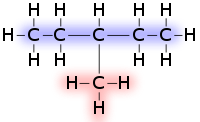
El grupo funcional alquilo (nombre derivado de alcano con la terminación de radical -ilo) es un sustituyente, formado por la separación de un átomo de hidrógeno de un hidrocarburo saturado o alcano,[1] para que así el alcano pueda enlazarse a otro átomo o grupo de átomos.
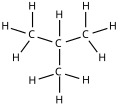
Se puede suponer que un grupo alquilo puede formarse a partir de un alcano, pero estos grupos no existen por separado (en ese caso se llaman radicales alquilo), o sea, los grupos alquilo no son compuestos en sí mismos, sino partes de compuestos mayores.[2] Los grupos alquilo siempre se encuentran unidos a otro átomo o grupo de átomos, como en el gráfico de la derecha. A pesar de ello, es interesante considerarlos como partes que se pueden separar pues esto facilita la nomenclatura de los compuestos orgánicos y la comprensión del mecanismo de ciertas reacciones como la transmetilación.
Así, si separamos un hidrógeno de un metano (CH4) nos quedaría el grupo metilo (CH3-), pero este grupo no puede estar aislado pues en ese caso sería el radical metilo (CH3) altamente reactivo. Son muy frecuentes y aparecen como sustituyentes o unidades estructurales en muchos compuestos orgánicos.[3]
Serie homóloga
[editar]El grupo metilo forma parte de una "familia" de sustituyentes orgánicos llamados grupos alquilo alquímicos, ya que siguen un mismo patrón: solo contienen átomos de carbono e hidrógeno, unidos por enlace covalente sencillo en la serie homóloga -(CH2)n-H con fórmula molecular CnH2n+1 y al ser un grupo funcional forman parte de una molécula mayor. Cuando un grupo metilo se separa de una molécula, se convierte en un radical metilo.
Si los ordenamos de menor a mayor número de átomos de C, los cuatro primeros tienen nombres específicos (metilo, etilo, propilo y butilo) mientras que los que siguen solo se denominan con la raíz griega según el número de carbonos (pent-, hex-, etc.) y la terminación -il(o).
| Radical | Fórmula simplificada |
Fórmula semi-desarrollada |
|---|---|---|
| Metilo | -CH3 | -CH3 |
| Etilo | -C2H5 | -CH2-CH3 |
| Propilo | -C3H7 | -CH2-CH2-CH3 |
| Butilo | -C4H9 | -CH2-CH2-CH2-CH3 |
| Pentilo | -C5H11 | -CH2-CH2-CH2-CH2-CH3 |
| Hexilo | -C6H13 | -CH2-CH2-CH2-CH2-CH2-CH3 |
| Heptilo | -C7H15 | -CH2-CH2-CH2-CH2-CH2-CH2-CH3 |
| Octilo | -C8H17 | -CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH3 |
| Nonilo | -C9H19 | -CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH3 |
| Decilo | -C10H21 | -CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH3 |
Estructura
[editar]Hay que distinguir entre grupos alquilo de cadena recta y de cadena ramificada según la geometría de la cadena alquílica, es decir, la ausencia de ramificaciones (como en el grupo propil), o la presencia de las mismas (en el grupo isopropil).
Según que el átomo de hidrógeno supuestamente eliminado pertenezca a un carbono terminal (carbono primario) o intermedio (carbono secundario, etc..) podemos distinguir entre grupos alquino primarios, secundarios y terciarios, ya que dicho átomo de H que falta definirá el carbono de unión entre el grupo alquilo y el resto de la molécula.
En la tabla inferior se observan dos grupos derivados del butano, eliminando el H en un carbono primario (n-butil) o secundario (sec-butil); y dos derivados del metilpropano, eliminando el H en un C primario (isopropil) o terciario (ter-butil).
| Grupo funcional | Símbolo | Fórmula | Estructura | Prefijo | Sufijo | Ejemplo |
|---|---|---|---|---|---|---|
| Grupo metilo | Me | -CH3 | 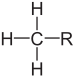
|
metil- | -metano | 
|
| Grupo etilo | Et | -CH2CH3 | 
|
etil- | -etano | |
| Grupo propilo | n-Pr | -CH2CH2CH3 | 
|
propil- | N-propano | |
| i-Pr | -CH(CH3)2 | 
|
isopropil- | isopropano | 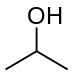
| |
| Grupo butilo | _ | -CH2CH2CH2CH3 | butil- | -butano | ||
| _ | -CH2CH(CH3)2 | 
|
isobutil- | -isobutano | 
| |
| _ | -CH(CH3)CH2CH3 | 
|
sec-butil- | _ | ||
| _ | -C(CH3)3 | 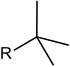
|
tert-butil- | _ | ||
| Grupo pentilo | _ | -CH2CH2CH2CH2CH3 | 
|
pentil- | -pentano |
Etilo
[editar]
En química el grupo etilo (-C2H5) es un grupo alquilo que resulta de la pérdida de un hidrógeno del etano (C2H6).
La etilación es la introducción en un compuesto de un grupo funcional etilo, lo que origina un nuevo compuesto. Dependiente de los estados de oxidación de los compuestos involucrados, la etilación puede conllevar un aumento sensible y contundente en la estabilidad molecular de los compuestos resultantes.
Metilo
[editar]

El grupo funcional metilo (CH3-) es el más simple de los grupos alquilo. Es de carácter hidrófobo que consta de un átomo de carbono (C) y tres de hidrógeno (H). Es siempre una parte o fracción, generalmente un sustituyente, dentro de una molécula orgánica mayor.[4] Para esta acepción, ver este mismo artículo.
No confundir con el radical metilo, (CH3), el cual deriva del metano (CH4) por eliminación de un átomo de hidrógeno,[5] posee un electrón desapareado[6] y existe como unidad molecular independiente aunque su vida media sea muy corta.
Nomenclatura
[editar]El grupo metilo es una ramificación o resto alquilo de un solo átomo de carbono en una cadena carbonada mayor o a un grupo funcional dentro de un compuesto orgánico. Es muy frecuente y se representa por CH3- (a veces, se abrevia como Me-) pero siempre forma parte de una molécula.
Cuando se nombra un grupo metilo dentro del nombre de un compuesto, se omite la "o" final; por ejemplo, 2-metilpropano.
Por otro lado, si hay más de un grupo metilo en un compuesto se nombra la cadena principal según el número de carbono que contenga, y los radicales o sustituyentes se nombran delante, con el prefijo "di-" si aparecen dos grupos metilo, como en 1,3-dimetilbutano; "tri-" si aparecen tres grupos metilo, como en 2,2,3-trimetilbutano; "tetra-" si aparecen cuatro grupos metilo como en 2,2,3,3-tetrametilbutano,...y así sucesivamente, como en los siguientes ejemplos.
| Fórmula estructural | Fórmula semidesarrollada |
Fórmula abreviada (poco usada) |
Nombre |
|---|---|---|---|
 |
CH3- | Me- | Grupo metilo (nunca existe aislado) |
 |
CH3-Cl | MeCl | Cloruro de metilo o clorometano |

|
CH3-OH | MeOH | Alcohol metílico o metanol |
 |
CH3-CH(CH3)-CH3 | 2-metilpropano o metilpropano | |
 |
CH3-CH(CH3)2-CH2-CH3 | 2,2-dimetilbutano |
Propiedades
[editar]- Es un grupo muy estable que se mantiene intacto en muchas reacciones químicas.
- Los enlaces carbono-hidrógeno poseen gran energía de disociación, superior a 100 kcal/mol, por lo que estos hidrógenos no poseen carácter ácido, no se separan del carbono. Esto contribuye a la escasa reactividad de los alcanos y de los grupos alquilo, como el metilo, dentro de una molécula frente a otros grupos funcionales más activos.
- Los enlaces carbono-hidrógeno no presentan polaridad debido a que el carbono y el hidrógeno poseen una electronegatividad parecida. Esto favorece la solubilidad de las sustancias con grupos alquilo en alcohol, acetona, éter y otros disolventes orgánicos pero no en agua.
- El átomo de C posee una hibridación sp3 (simetría tetraédrica) en el grupo metilo,[7] a diferencia del radical metilo, en el que tiene hibridación sp2 (simetría triangular plana).
Geometría
[editar]En tres dimensiones, los enlaces que vienen del átomo de carbono en el grupo metilo (CH3, o H3C) están simétricamente situados apuntando a los vértices de un tetrahedro imaginario el átomo de carbono está en el medio. El grupo metilo está libre para rotar alrededor del enlace carbono-nitrógeno. Tanto CH3 como H3C son solo representaciones bidimensionales como taquigráficas; el último es únicamente usado como una opción estética que el que la representa puede usar si piensa que el hidrógeno parecerá demasiado plegado contra el resto de la molécula.[8][9]
Propilo
[editar]
En química orgánica, el grupo propilo es un grupo alquilo con la fórmula química -C3H7. Es la forma sustituyente del alcano propano. Un sustituyente propilo es usualmente representado en química orgánica con el símbolo Pr (no debe confundirse con el elemento praseodimio).
Hay dos formas isoméricas de propilo:
- con el sustituyente unido a uno de los carbonos extremos (llamada prop-1-il en la nomenclatura IUPAC, o n-propilo (Pr-n) en el viejo sistema de nomenclatura); y
- con el sustituyente unido al carbono de al medio (llamada prop-2-il en el sistema IUPAC, o isopropilo en el sistema viejo).
Además hay una tercera forma, cíclica, llamada ciclopropilo, o c-propilo. Esta no es isomérica con las otras dos formas, teniendo la fórmula química -C3H5.
- Ejemplos

- Esto es etanoato de propilo, un éster. El grupo propilo se añade a la molécula después del oxígeno de al medio.
Véase también
[editar]Referencias
[editar]- ↑ http://goldbook.iupac.org/A00228.html IUPAC Recommendations 1995: Glossary of class names of organic compounds and reactivity intermediates based on structure. Pág. 1314
- ↑ Química orgánica. John McMurry. 6ª ed. Cengage Learning Editores, 2005. ISBN 9706863540. Pág. 77
- ↑ Química orgánica. Robert Thornton Morrison, Robert Neilson Boyd. 5ª ed. Pearson Educación, 1998. ISBN 9684443404. Pág. 86
- ↑ Química para el nuevo milenio. John William Hill, Doris K Kolb 8ª ed. Pearson Educación, 2000. ISBN 9701703413. Pág. 230
- ↑ The Free Dictionary Definición del término metilo.
- ↑ Química orgánica simplificada. Rudolph Macy. Editorial Reverté. Barcelona, 1976. ISBN 8429173315.Pág. 65.
- ↑ Química: la ciencia central. Theodore L. Brown, Bruce E. Bursten, Julia R. Burdge. 9ª ed. Pearson Educación, 2004. ISBN 9702604680. Pág.1024
- ↑ «Copia archivada». Archivado desde el original el 14 de mayo de 2013. Consultado el 16 de julio de 2013.
- ↑ http://www.chemistry24.com/college_chemistry/naming-chemicals.html








