Loading AI tools

iBet uBet web content aggregator. Adding the entire web to your favor.
Link to original content: http://wikiwand.com/es/articles/Microtúbulos

estructuras celulares poliméricas De Wikipedia, la enciclopedia libre
Los microtúbulos son estructuras celulares formadas por polímeros proteicos, de 25 nm de diámetro exterior y unos 12 nm de diámetro interior, con longitudes que varían entre unos pocos nanómetros a micrómetros,[1] que se originan en el Centro organizador de microtúbulos (MTOC en inglés) y que se extienden a lo largo de todo el citoplasma. Se hallan con diferentes características en las células eucariotas y en las procariotas. Están formados por la polimerización de un dímero de dos proteínas globulares, la tubulina alfa y la tubulina beta.[2]
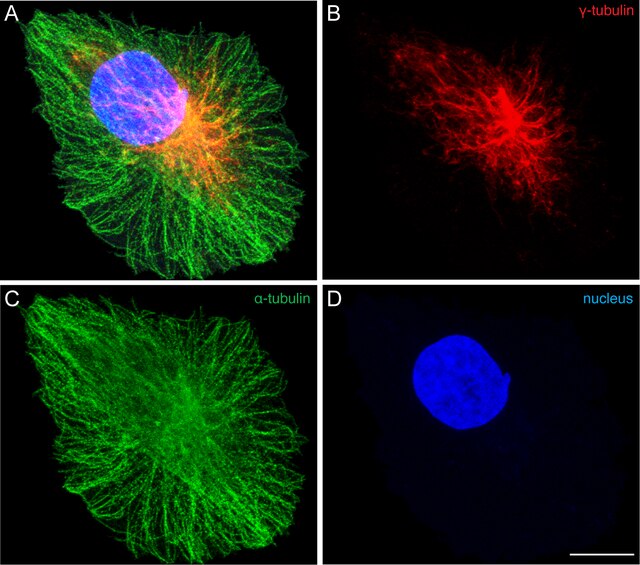

Los microtúbulos intervienen en diversos procesos celulares que involucran desplazamiento de vesículas de secreción, movimiento de orgánulos, transporte intracelular de sustancias, así como en la división celular (mitosis y meiosis) y que, junto con los microfilamentos y los filamentos intermedios, forman el citoesqueleto. Además, constituyen la estructura interna de los cilios y los flagelos.
Los microtúbulos se nuclean y organizan en los centros organizadores de microtúbulos (MTOC), como pueden ser el centrosoma o los cuerpos basales de los cilios y flagelos. Estos centros organizadores pueden poseer centríolos o no.
Además de colaborar en el citoesqueleto, los microtúbulos intervienen en el tránsito de vesículas (véase la dineína o la cinesina), en la formación del huso mitótico mediante el cual las células eucariotas segregan sus cromátidas durante la división celular, y en el movimiento de cilios y flagelos.

Los microtúbulos son heteropolímeros de α- y β-tubulina, los cuales forman dímeros, que son su unidad estructural.[3] Los dímeros polimerizan en 13 protofilamentos, que luego se agregan lateralmente para formar estructuras cilíndricas huecas. Para polimerizar se requiere la presencia de dímeros a una concentración mínima determinada denominada concentración crítica, aunque el proceso se acelera por la adición de núcleos, que son elongados.

Una importante característica de los microtúbulos es su polaridad. La tubulina polimeriza por adición de dímeros en uno o ambos extremos del microtúbulo. La adición es por unión cabeza con cola, en la formación de los protofilamentos. Así, se forman filas sesgadas de monómeros de α y β-tubulina en la pared, lo que provoca una polaridad global al microtúbulo. Debido a que todos los protofilamentos de un microtúbulo tienen la misma orientación, un extremo está compuesto por un anillo de α-tubulina (denominado extremo -) y, el opuesto, por un anillo de β-tubulina (denominado extremo + plus).[4]
Los microtúbulos bacterianos tienen un diámetro menor que los eucariotas pero presentan la misma estructura básica. En la bacteria los homólogos de las tubulinas, las proteínas tubulina A bacteriana (BtubA en inglés) y tubulina B bacteriana (BtubB) también forman microtúbulos. Los microtúbulos bacterianos muestran protofilamentos que están ordenados y que presentan interacciones similares a los eucariotas. Los microtúbulos bacterianos están compuestos de solo cinco protofilamentos, en lugar de los 13 presentes en los eucariotas.[5][6]
La polimerización de los microtúbulos se nuclea en un centro organizador de microtúbulos. En ellos existe un tipo de tubulina, llamada γ-tubulina, que actúa nucleando la adición de nuevos dímeros, con intervención de otras proteínas reguladoras. Así, se considera la existencia de un complejo anular de γ-tubulina, siempre situado en el extremo - del microtúbulo.[7]

Durante la polimerización, ambas unidades de tubulina se encuentran unidas a una molécula de guanosín trifosfato.[3] El GTP desempeña una función estructural en la α-tubulina, pero es hidrolizado a GDP en la β-tubulina. Esta hidrólisis modula la adición de nuevos dímeros. Así, el GTP se hidroliza tras un lapso del tiempo, lo que permite que, si la adición de dímeros es rápida, se forme en el extremo (+) un casquete de β-tubulina unida a GTP, mientras que, de ser lenta, lo que se expone es tubulina unida a GDP. Pues bien: esta unión a uno u otro nucleótido es la que determina la velocidad de polimerización o despolimerización del microtúbulo. Así, un casquete en el extremo (+) con GTP favorece la elongación, mientras que uno de GDP, la despolimerización.[8]
.
Ahora bien, este proceso, de adición o no de nuevos monómeros, depende de la concentración de dímeros de αβ-tubulina en la solución; si su concentración es mayor de un parámetro conocido como concentración crítica (Cc) (que es la constante de equilibrio de disociación de los dímeros del extremo del microtúbulo), el microtúbulo crece, y si es menor, decrece. Y según la presencia de un casquete de GTP o GDP, la Cc es distinta, lo cual define que el extremo (+) y (-) tengan valores distintos, lo que a su vez redunda que la actividad dinámica del extremo (+) sea mayor debido a una menor Cc específica. El microtúbulo, por tanto, puede crecer por ambos extremos o solo por uno, dependiendo de la concentración de dímeros de αβ-tubulina. La interacción del extremo (-) con el MTOC disminuye mucho su actividad.
Existen otras proteínas denominadas MAP (Microtubule Associated Protein) o proteínas asociadas a microtúbulos. Se considera que colaboran en el ensamblaje de los dímeros para formar microtúbulos.
Las MAP se clasifican por su peso molecular en dos grupos:
También denominadas proteínas τ(tau). Recubren al microtúbulo y establecen uniones con microtúbulos adyacentes.
Se conocen 4 tipos de MAP diferentes: MAP-1, MAP-2, MAP-3, MAP-4 Las MAP-1 comprende por lo menos 3 proteínas diferentes: A, B y C. La C es importante en el transporte retrógrado de vesículas y se denomina dineina citoplasmática. Las MAP-2 están en las dendritas y el cuerpo de las neuronas, donde se asocian a otros filamentos. Las MAP-4 se encuentran en la mayoría de las células y estabilizan los microtúbulos.
Resumen global de dichas propiedades:
Estas características derivan en la existencia de una inestabilidad dinámica de los microtúbulos, que consiste en que, en una misma célula, algunos microtúbulos están despolimerizándose (catástrofe) y otros elongándose (rescate).
Existen proteínas que aprovechan la hidrólisis de ATP para generar energía mecánica y desplazar sustancias sobre microtúbulos. Estas son la dineína, transportador retrógrado, y la kinesina, transportador anterógrado.

Existen una gran cantidad de drogas capaces de unirse a la tubulina, modular su estado de activación y de este modo interferir con la dinámica microtubular a concentraciones intracelulares mucho más bajas que la de tubulina. De este modo, las células detienen su ciclo celular y pueden conducir a la muerte celular programada o apoptosis. Los compuestos que modulan la actividad de tubulina pueden dividirse de forma general en dos grandes grupos: En primer lugar están los inhibidores de su polimerización, como la colchicina[9] y la vincristina,[10] que se unen a ésta impidiendo que forme microtúbulos. Por otro lado, están los agentes estabilizantes de microtúbulos (MSAs), como el paclitaxel (conocido comercialmente como taxol)[11] y el docetaxel,[12] los cuales se unen preferentemente a la tubulina ensamblada, minimizando la disociación de la tubulina-GDP de los extremos de los microtúbulos e induciendo el ensamblaje de la tubulin-GDP normalmente inactiva.
Los fármacos moduladores de la polimerización de microtúbulos han sido muy usados en la terapia antitumoral. Al ser indispensables para la mitosis y detenerla, se logra actuar contra el tumor, pero también se ven afectados aquellos tejidos en rápida proliferación (médula ósea, mucosa intestinal...). El éxito clínico del paclitaxel y el docetaxel ha conducido a la búsqueda de nuevos compuestos con el mismo mecanismo de acción y al descubrimiento en los últimos años de una gran cantidad de agentes estabilizantes de microtúbulos con al menos dos sitios de unión distintos.
Además de su papel estructural como componente del citoesqueleto (junto con la actina y los filamentos intermedios), los microtúbulos están relacionados con procesos biológicos.
El citoesqueleto de microtúbulos es esencial durante los procesos morfogenéticos del desarrollo de los organismos. Por ejemplo, durante la embriogénesis en la mosca de la fruta, Drosophila melanogaster, se requiere de una red de microtúbulos intacta y polarizada dentro del Oocito a fin de establecer los ejes del huevo; de este modo, las señales entre las células foliculares y las del Oocito (como los factores semejantes al TGF-alfa) provocan la reorganización de los microtúbulos situando su extremo menos en la zona anterior del oocito, lo que polariza la estructura y conlleva la aparición de un eje anterior-dorsal.[13] Esta implicación en la arquitectura del cuerpo también se da en mamíferos.[14]
Otro campo en el cual los microtúbulos son esenciales es la formación del sistema nervioso en vertebrados superiores; en ellos, la dinámica de la tubulina y de las proteínas asociadas (como las MAPs) es controlada con precisión a fin de desarrollar la base neuronal del cerebro.[15]
El citoesqueleto celular es un elemento dinámico que actúa a muchos niveles en la célula: además de dotarla de una forma determinada y de vertebrar el tráfico de vesículas y orgánulos, puede influir en la expresión génica. No obstante, las vías celulares (esto es, los mecanismos de transducción de señales) que intervienen en esta comunicación son muy poco conocidos. No obstante, se ha descrito la relación entre la despolimerización de microtúbulos mediada por fármacos y la expresión específica de factores de transcripción y, por ello, la expresión diferencial de los genes dependientes de la presencia de estos factores.[16] Esta comunicación entre el citoesqueleto y la regulación de la respuesta celular está también relacionada con la generación de factores de crecimiento: por ejemplo, esta relación existe para el factor de crecimiento de tejido conectivo.[17]
En la terapia contra el cáncer este hecho tiene vital importancia pues el medicamento antitumoral paclitaxel posee como diana el citoesqueleto de microtúbulos, y es precisamente la interacción de este último con elementos que modulan el ciclo celular lo que provoca, en presencia del antitumoral, una serie de fallos celulares en las células cancerosas que conducen a su muerte celular programada o apoptosis.[18]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.