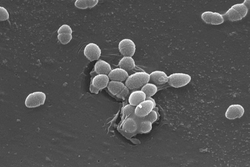
Enterococcus faecalis
| Enterococcus faecalis | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| Enterococcus faecalis (Orla-Jensen 1919) Schleifer & Kilpper-Bälz 1984 | |||||||||||||||
Enterococcus faecalis é uma bactéria Gram-positiva comensal (flora normal) do sistema digestivo humano e de outros mamíferos. Amplamente encontrada no ambiente, pode causar infecção urinária, meningite e bacteremia, especialmente em ambientes hospitalares. [1]
Costumava ser classificado como Streptococcus faecalis grupo D.
Fisiologia
[editar | editar código-fonte]E. faecalis são bactérias Gram-positivas, podem ser móveis, facultativamente anaeróbicas, catalisam diversas fontes de energia e normalmente encontradas no sistema digestivo e no trato genital feminino. Podem ser encontrados no solo, na água e nas plantas. Formam cadeias curtas e pares e podem parecer cocobacilares em alguns cultivos. E. faecalis sobrevivem a ambientes aversivos, incluindo pH extremamente alcalino (9,6) e elevadas concentrações de sal. Resistem a sais biliares, detergentes, metais pesados, etanol, azida e a dessecação. Podem crescer no intervalo de 10 a 45 °C e sobreviver a temperaturas de 60 °C durante 30 min.[2]
Epidemiologia
[editar | editar código-fonte]E. faecalis constituem 85 a 90% das espécies de Enterococcus identificados nos humanos, sendo essa espécie a menos propensa ao desenvolvimento de resistência a antibióticos. E. faecium é o menos prevalente, de 5 a 10%, mas apresenta maior propensão ao desenvolvimento de resistência.
Resistências
[editar | editar código-fonte]A emergência desse patógeno nas últimas duas décadas, entre muitos fatores, se deve em parte à sua resistência intrínseca aos antimicrobianos comumente utilizados, como: aminoglicosídeos, aztreonam, cefalosporinas, clindamicina, oxacilina.[3]
E. faecium é menos sensível aos antimicrobianos beta-lactâmicos do que E. faecalis devido à baixa afinidade das proteínas de ligação da penicilina (PBP) a esses compostos.[3]
Os enterococos possuem:[4]
- Alta resistência a penicilinas (oxacilina, meticilina), clindamicina, cefalosporinas e sulfametoxazol/trimetoprim;
- Baixo nível de resistência, em relação a agentes ativos na parede celular: penicilina e vancomicina;
- Baixo nível de resistência aos aminoglicosídeos: estreptomicina CIM usual de 8 a 256 μg/mL; e gentamicina e tobramicina CIM usual de 4 a 128 μg/mL.
- Resistência à ampicilina e penicilina — não-beta-lactamase-mediada: devido à alteração de proteínas de ligadoras de penicilina (PBP), mais frequente;
- Resistência à ampicilina e penicilina — beta-lactamase-mediada: a resistência à ampicilina e penicilina também pode ser atribuída à produção de beta-lactamase, descrita quase que exclusivamente para o E. faecalis e atribuída, na maioria dos casos, à aquisição do operon responsável pela produção de beta-lactamase do Staphylococcus aureus;
- Altos níveis de resistência a aminoglicosídeos (HLAR, high-level resistance to aminoglycosides): resistência plasmídeo-mediada com a aquisição de novos genes que codificam enzimas que promovem modificações nos aminoglicosídeos.
- Resistência à vancomicina está associada a alterações na parede celular (modificação dos precursores de parede bacteriana impedindo a ligação da droga em seu sítio de ação), pode ser mediada por plasmídeo ou cromossomo. O VRE foi reconhecido em 1988 e é responsável por mais de 20% das infecções enterocócicas nos EUA. No Brasil, foi descrito pela primeira vez em 1996, em Curitiba. Estudos recentes já mostram mais de 15% de resistência à vancomicina em alguns hospitais brasileiros. A emergência dessa resistência pode estar relacionada ao aumento do uso de vancomicina, nos últimos 20 anos, decorrente da terapêutica das infecções por MRSA.
Principais Fenótipos de Resistência[5]
[editar | editar código-fonte]Os três fenótipos de resistência encontrados são mediados pelos genes VanA, VanB, VanC e os menos frequentes, VanD e VanE.
O sinergismo entre ampicilina, penicilina ou vancomicina e um aminoglicosídeo pode ser determinado para Enterococcus spp., desde que realizado o teste para níveis altos de resistência a aminoglicosídeos (gentamicina 500 μg/mL e estreptomicina 1 000–2 000 μg/ml).
Tratamento
[editar | editar código-fonte]No Brasil, há ainda uma grande predominância de cepas de VRE da espécie E. faecalis sensíveis a ampicilina e aminoglicosídeos (estreptomicina), e que podem ser tratadas com esses antimicrobianos. Apesar disso, relatos recentes têm demonstrado um aumento na incidência de E. faecium nos hospitais, com um perfil de resistência mais amplo. Quando as infecções são causadas por Enterococcus spp. resistentes aos glicopeptídeos, penicilinas e aminoglicosídeos, as opções se restringem à linezolida e, mais recentemente, às glicilciclinas (tigeciclina).
Referências
- ↑ Ryan KJ, Ray CG (editors) (2004). Sherris Medical Microbiology 4th ed. [S.l.]: McGraw Hill. pp. 294––5. ISBN 0-8385-8529-9
- ↑ https://microbewiki.kenyon.edu/index.php/Enterococcus_faecalis
- ↑ a b «Módulo 3: Resistência Microbiana - Mecanismos e Impacto Clínico». www.anvisa.gov.br. Consultado em 3 de dezembro de 2017
- ↑ «Módulo 3: Resistência Microbiana - Mecanismos e Impacto Clínico». www.anvisa.gov.br. Consultado em 3 de dezembro de 2017
- ↑ «Módulo 3: Resistência Microbiana - Mecanismos e Impacto Clínico». www.anvisa.gov.br. Consultado em 3 de dezembro de 2017