抗精神病薬
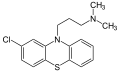
抗精神病薬(こうせいしんびょうやく、英語: Antipsychotics)は、広義の向精神薬の一種[注釈 1]で、主に統合失調症などの症状を緩和する精神科の薬である[1][2]。過去には、神経遮断薬 (Neuroleptics)[3]、あるいはメジャートランキライザー (Major tranquilizers) とも呼ばれ、1950年代には単にトランキライザーと呼ばれた。薬事法における劇薬に指定されるものが多い。抗精神病薬は、それ以外にも幅広い精神障害に使用される。精神科の薬というのはこの抗精神病薬のことを指す。代表的な薬品として、クロルプロマジンやハロペリドールなどがある。
概要
[編集]抗精神病薬は大きく2分類することができ、古い定型抗精神病薬と、新世代型の非定型抗精神病薬がある。非定型抗精神病薬は、双極性障害のうつ状態やうつ病にも適応がある薬がある。非定型抗精神病薬は、従来の定型抗精神病薬と比較してドーパミンD2受容体拮抗作用に加えてセロトニン5HT2A受容体拮抗作用を有したり、「緩い」ドーパミンD2受容体拮抗作用を有するなどの特徴をもった薬剤である。非定型抗精神病薬は、錐体外路症状、口が渇く、便秘といった副作用が少なく、統合失調症の陰性症状にも効果が認められる場合があるとされる。しかし#定型対非定型節に見られるように、大規模な試験による分析によれば、非定型抗精神病薬が定型抗精神病薬よりも優れているという根拠は乏しい。
副作用として、口渇、便秘、無意識的に身体が動く錐体外路症状や、肥満といった代謝の異常、母乳が出るといった高プロラクチン血症などがある。代謝の異常は、特に非定型抗精神病薬に特徴的である。抗精神病薬を服用している患者の代謝のチェックが日常的に適切に行われていないことが多く、約90%の患者が1つ以上の代謝性の危険因子を持ち、約30%がメタボリックシンドロームである[4]。さらに抗精神病薬の使用は高い無職率の原因となっている[5]。また服薬を中断する場合#離脱症状が生じる可能性がある。#有効性節以下で示されるが、効果がなかったり副作用のため服薬の中止が多い薬剤である。
抗精神病薬の過剰処方が問題となっている。投与量の増大に伴う治療効果は頭打ちになるが、副作用発現率は上昇していくため、世界保健機関(英語: World Health Organization、略称:WHO)および英米の診療ガイドラインでは単剤療法を推奨している[1]。日本でも2010年に、抗精神病薬の種類が2種類以下である場合に診療報酬が有利になる改定が行われた[6]。厚生労働省自殺・うつ病等対策プロジェクトチームが「統合失調症に対する抗精神病薬多剤処方の是正に関するガイドライン」の策定を計画しており[7]、2013年10月にSCAP法という減薬ガイドラインが公開された[8]。抗精神病薬の大量処方からの減量は、過感受性精神病という離脱症状による精神症状の悪化を引き起こす可能性があり注意が必要である[9]。
抗精神病薬の使用は脳の容積を減少させるかについてはさらなる研究を要する[10]。抗精神病薬の使用は若年認知症発症の危険因子である[11]。
医療用途
[編集]統合失調症に用いるのが典型的な用途である[1]。抗精神病薬は、ドーパミン拮抗薬(ドーパミン・アンタゴニスト)で、主な作用は脳内の神経伝達物質であるドーパミンの遮断である。主に、中脳辺縁系のドーパミン作動性ニューロンのドーパミンD2受容体を遮断する。そのことによって、妄想や幻覚といった精神症状を軽減させる。PET(ポジトロン断層法)での研究から、高プロラクチン血症や錐体外路などの副作用が生じるよりも少ない量で有効な反応がみられることが明らかになっている[12]。
単に適応が認められていないばかりでなく、小児や高齢者では死亡リスクを高めることが実証されているために、適応外使用の違法なマーケティングに対し、非定型抗精神病薬のエビリファイ(アリピプラゾール)、ジプレキサ(オランザピン)、セロクエル(クエチアピン)、リスパダール(リスペリドン)と罰金の史上最高額を塗り替えている[13]。
いずれにせよ、各々の薬剤の特徴を考え、標的症状の性質と照らし合わせながらエビデンスに基づいた薬剤使用が望まれる。また、いたずらな多剤併用は避け、可能な限り単剤投与を心がけるべきであり、WHOガイドラインでも「一度に1種類の抗精神病薬を処方する」という立場である[1]。
統合失調症
[編集]WHOのガイドラインでは、急性精神病の管理に抗精神病薬の治療を開始するとしている[1]。NICEガイドラインでは、統合失調症の治療第一選択肢は抗精神病薬および心理療法の併用である[14]。しかしプライマリケア医は、専門医の確定診断が無い限り、初回発症の段階で抗精神病薬を処方してはならないともしている[15]。
またNICEは発症防止、予防を目的とした抗精神病薬の投与は行ってはならないとも述べている[16]。
双極性障害
[編集]WHOガイドラインでは、双極性障害の急性躁エピソードの治療選択肢のひとつとして抗精神病薬が挙げられている[2]。抗精神病薬の処方を中断する場合は、最低4週間かけ徐々に減薬する必要がある[17]。
認知症
[編集]認知症患者のBPSD管理に用いられる。処方は強い精神病症状、暴力、攻撃性、行動障害の症状に限り、正しい利用に努め、低用量にて副作用を監視しながら慎重に投与すべきである[18][19]。
NICEの2006年ガイドラインは、BPSDに対して薬物介入を第一選択肢とするのは、深刻な苦痛または緊急性のある自害・他害リスクのある場合に限らなければならないとしている[18]。
その他
[編集]脳の興奮状態を抑制させる作用を利用して、抗不安薬では取り除けないような強度の不安や極度のうつ状態、不眠に対する対処薬としても利用される場合もある。また、ドーパミン遮断作用を応用し、嘔気・嘔吐などの消化器症状や吃逆の対症薬として利用される場合もある。
アメリカ精神医学会(英語: American Psychiatric Association、略称:APA)は成人の不眠症に対し、抗精神病薬を継続的にファーストライン治療としてはならないと勧告している[20]。NICEは不安障害に対し、抗精神病薬は特別の事情 (specifically indicated) を除き処方してはならないとし、かつルーチン処方を禁じている[21]。
自閉症の興奮状態に、リスパダールは処方される。
副作用
[編集]抗精神病薬は様々な副作用に結びついている。有害事象が原因で多くの人々(対照臨床試験で約3分の2)が服薬を中止することは、よく認識されている[22]。
作用機序別
[編集]ドーパミンD2受容体遮断作用による錐体外路反応は以下のようなものを含む、急性ジストニア、アカシジア、パーキンソン症候群(硬直と振戦)、遅発性ジスキネジア、頻脈、低血圧、勃起不全、傾眠、発作、強烈な夢あるいは悪夢、高プロラクチン血症[1][23]。高プロラクチン血症は、無月経、乳汁分泌、陰萎などを含む。
ムスカリン性アセチルコリン受容体遮断作用には、便秘、眼のかすみ、口渇などが挙げられる。ヒスタミンH1受容体遮断作用などによる眠気、鎮静、体重増加などが挙げられる。α1アドレナリン受容体遮断作用による低血圧、めまい、射精障害、おそらくは中枢における過度のドーパミン抑制によって誘起されると言われている悪性症候群などがある。
また特に非定型抗精神病薬においては体重増加、糖尿病という副作用が見られることがある。非定型抗精神病薬の服薬にあたっては、定期的な血糖値検査が必要とされる。
抗精神病薬の副作用はいくつかの異なる薬によって管理することができる。例えば、抗コリン薬は、抗精神病薬による運動性の副作用を軽減するのに用いられる[24]。副作用の一部は、薬が長期間用いられた場合にのみ生じる。
精神病のない「健常」人における抗精神病薬の投与は、いわゆる統合失調症の「薬原性陰性症状」(例えば情緒と意欲の問題)を生じさせる[25]。
ドーパミンD2受容体遮断作用
[編集]いわゆる錐体外路症状(英語: extrapyramidal symptom、略称:EPS)と言われるものである[1]。パーキンソン症候群、不随意運動としてアカシジア、ジストニア、ジスキネジアが有名である[1]。命にかかわる重篤な副作用としては悪性症候群が知られている[1]。内服後、どの程度の時間経過で出現するかによって早発症状、遅発症状に分けられる。遅発性が薬物の減量で改善しないこともあり治療に工夫が必要となる。また、高プロラクチン血症による女性化乳房も気になりやすい副作用である。
- 遅発性ジストニア(tardive dystonia, TDt)
異常姿勢が一般的である。眼球回転発作、ピサ症候群、メージュ症候群、書痙といった亜型も知られている。感覚トリックといわれ、自分では拘縮で動かせないが他動的には動かせるなど特徴的な不随意運動である。抗コリン薬、筋緊張治療薬、ビタミンE、抗てんかん薬を用いることがある。非定型抗精神病薬で治療することもある。
- 内分泌障害
高プロラクチン血症による女性化乳房も一般的だが、水中毒など緊急を要する副作用もある。
ムスカリン性アセチルコリン受容体遮断作用
[編集]いわゆる抗コリン作用である。口渇、便秘、排尿障害の他、視力調節障害や緑内障の悪化が認められる。
アドレナリンα1受容体遮断作用
[編集]起立性低血圧、射精障害、勃起障害、循環器障害が有名である。また外因性カテコラミンが併用禁忌となる場合もある。
ヒスタミンH1受容体遮断作用
[編集]鎮静作用、体重増加など。
死亡リスクの増加
[編集]いくつかの研究は、抗精神病薬の使用が平均余命の減少に結びついていることを見出し、さらなる研究が必要であると論じた[26][27]。
2005年にアメリカ食品医薬品局(FDA)は、非定型抗精神病薬が、高齢の認知症患者の死亡率を1.6-1.7倍に高めているため警告を行った[28]。FDAは、包装にその旨の警告を追加した[29]。特に認知症患者では、投与をはじめた直後の死亡リスクが高い[30]。日本の添付文書でも、自殺関連の既往歴のある患者に対して悪化させるおそれの旨が記載されている。
2018年のシステマティックレビューは352件のランダム化比較試験から解析し、全死亡率に違いはないため統合失調症では死亡率増加はないとしたが、認知症や高齢者に対象を絞ると死亡率増加が認められた[31]。
心臓発作
[編集]高齢者では、非定型抗精神病薬によって、投与から最初の30日間の心臓発作のリスクは2.19倍で、60日では1.62倍、90日では1.36倍、1年では1.15倍である[32]。
肺炎
[編集]高齢者では、定型、もしくは非定型の抗精神病薬ともに肺炎の危険性を高め、特に非定型では致命的な肺炎の危険性が約6倍である[33]。
脳容積の減少
[編集]2011年2月、抗精神病薬で治療された統合失調症患者で、脳組織の僅かな減少が報告された[34][35]。脳の容積は、罹患期間と抗精神病薬の投与量の両方で逆の相関関係があった。病気の重症度あるいはほかの物質の乱用との相関はなかった。 付随論説は述べる:「この知見は、統合失調症に対する治療としての抗精神病薬の使用の中断を示していると解釈すべきではない。しかし、それらは治療目標の達成に必要な最小の量で処方すること[および]転帰を改善するための非薬理学的手法の追加を検討すること、個々の患者でのこれらの医薬品の利益と有害影響を注意深く監視する必要があることを強調している」[34][36][37][38]マカクザルにおける抗精神病薬の継続使用は、脳の総体積の10%の減少を示した[39]。
さらに2012年に、多面的メタアナリシスが行われ43の脳画像研究を調査し、75%に容積の減少が見られ抗精神病薬による薬物治療を受けた患者に多く、異常のない25%は薬物治療のない患者であった[40]。
2017年3月のメタアナリシスは、抗精神病薬と脳の変化について、ほとんど研究で統計的に有意な変化でないが小さな研究が多く、決定的な結論のためにさらなる研究を要するとした[10]。
抗精神病薬は若年認知症の危険因子であり、ハザード比は、アルコール依存4.82、脳卒中2.96、抗精神病薬の使用2.75、うつ1.89である[11]。
異常運動
[編集]神経遮断薬 (Neuroleptic) は、抗精神病薬の古い呼称だが、この医薬品が引き起こす異常運動を強調するには適切である[3]。パーキンソンニズム、悪性症候群、ジストニア、アカシジア、ジスキネジアがある[3]。
- より重篤な副作用の一つは遅発性ジスキネジアで、これを患う場合、唇、顔、足、胴の、反復的で不随意で無目的な運動を示す(永続的で治療法がない)[1]。古い定型の抗精神病薬のほうが遅発性ジスキネジアを発現させる危険性が大きいと考えられているが、新しい抗精神病薬もこの障害を引き起こすことが知られている。
- 悪性症候群、体温調節中枢が機能しなくなることが原因で、患者の体温はすぐに危険な域に上がる。
- 薬剤誘発性のパーキンソン症候群は、ドーパミンD2受容体の遮断に起因する。非定型薬よりも定型薬のほうが引き起こす危険性がある。
- 低体温は、量の変動によって起こりやすく、副作用監視機関のデータからは文献で示された有病率より10倍高いと考えられる[41]。
- アカシジア。足がムズムズするなどして、じっとしていることができない。定型、非定型のどちらも原因になる[42]。遅発性アカシジアも生じうる[3]。
- ジストニア。神経系運動障害で、持続性筋収縮が反復運動や異常姿勢を引き起こす。遅発性ジストニアも生じうる[3]。
その他
[編集]抗精神病薬の一部の副作用に関する詳細は、以下である。
- 抗精神病薬、特に非定型薬は、グルコースの恒常性を調節する脳の部位と、膵β細胞上に発現するムスカリンM3受容体[43](インスリン分泌の主要調節因子[44])を遮断することでインスリン濃度の変化を招くようである。変化したインスリン濃度は、特に(アメリカの試験における)アフリカ系アメリカ人で、致命的な糖尿病と糖尿病性ケトアシドーシスの原因となる[45][46]。
- 抗精神病薬は、膵炎を引き起こす可能性がある[47]。
- いくつかの非定型抗精神病薬(特にオランザピンとクロザピン)は、ヒスタミン受容体[48]を占有し、食欲を調節する脳の部位における神経化学的な信号を変化させることに、部分的に起因する体重増加に関連している[49]。体重増加に関連した代謝系の副作用は糖尿病である[50]。証拠は、男性よりも女性のほうが非定型抗精神病薬の代謝系の副作用の影響を受けやすいことを示している[51]。
- クロザピンは、白血球数が危険な状態にまで減少する無顆粒球症の危険性があるために、定期的に血液検査を行い、兆候がないか検査する必要がある[52]。
- 多くの抗精神病薬の重篤な副作用の潜在性として、個人の発作閾値を低下させる傾向がある。とりわけクロルプロマジンとクロザピンである。フルフェナジン、ハロペリドール、ピモジド、リスペリドンは比較的危険性が低い。てんかんや脳損傷の既往歴がある場合、注意すべきである。
- 高プロラクチン血症。男女ともに乳房が大きくなり、乳を分泌する。血中のプロラクチンの異常な高水準が原因となる。
- 認知症患者における抗精神病薬が死亡率の増加に結びつくという議論の後、警告が包装に追加された[29]。このことについては、大規模な#訴訟が起こされている。
- FDAによる包装への追加は、2011年2月22日にも、新生児に異常な筋肉運動と薬物離脱症候群が起きることも追加された[53]。
- 知覚変容発作(Paroxysmal Perceptual Alteration)は、患者自身が発作であると認識していることが多く、突然の数分から数時間の、壁の黒いものが気になったり、周りが明るいといった、知覚過敏、外界の見え方の変化、空間構造の変化のような発作的な視覚的な変容を特徴とする[54]。うつ病や小児自閉症での抗精神病薬の使用でも生じ、抗精神病薬を中止すると生じなくなる[55][56]。ロラゼパムやアルプラゾラムなどの抗不安薬の頓用も有効である。[57]
離脱症状
[編集]抗精神病薬の離脱症状が、投与量の減少や投薬の中断によって発現する可能性がある。離脱症状は以下のようなものを含む:吐き気、嘔吐、食欲不振、下痢、鼻漏、発汗、筋肉痛、知覚障害、不安、興奮、情動不安、不眠症。精神的な離脱症状には、基礎疾患の再発として誤診が可能な精神病も含まれる。また逆に、離脱症状は再発の誘因となる可能性もある。離脱症状の良い管理は、抗精神病薬を中断するための個人の能力を高める。[58][59]
身体的な離脱症状として遅発性ジスキネジアが発現し、離脱の段階で徐々に弱まるか、あるいは持続する[60]。抗精神病薬からの離脱に関連した精神病は、過感受性精神病(supersensitivity psychosis)と呼ばれ、抗精神病薬によるドーパミン作動性受容体の遮断に起因する、脳のドーパミン受容体の数と感度の増加によるもので[61]、神経弛緩薬が除外されれば症状の悪化を誘発する[62]。同様に、抗精神病薬の効力はこの薬物耐性(drug tolerance)の発現が原因で時間とともに減少する可能性がある[59]。
離脱症状は、ある抗精神病薬を他のものに切り替えた場合にも生じることがある(おそらく力価の変動と受容体の活動に起因する)。そのような離脱症状は、コリン作動薬のリバウンド、賦活症候群、およびジスキネジアなどの運動症候群を含む。これらの有害事象は、抗精神病薬間での急な変更の間に起こりやすいので、抗精神病薬間で徐々に変更することでこれらの離脱症状を最小限にする[63]。一方を漸減し、もう一方を漸増する置換方法を、クロステーパーと呼ぶ[64]。『英国国民医薬品集』(British National Formulary)は、急性離脱症候群あるいは急な再発を避けるために、抗精神病薬を中断する時に段階的な使用中止を推奨している[65]。
抗精神病薬の離脱は困難である。おそらく、クロザピンの離脱は最悪である。多くの人々は離脱が不可能である[66]。
過感受性精神病
[編集]過感受性精神病は薬の減量と共に、つまり離脱症状として出現する精神症状の悪化であり、しばらくのちに症状が再燃する症状の再発とは異なる[9]。抗パーキンソン病薬は多剤大量処方による錐体外路症状に対して用いられているが、これにも離脱症状があるため抗精神病薬の調整が済んでから4週間ほどかけて減薬する[67]。多剤大量処方を是正している他の医師によれば、致命的な悪性症候群の危険性を避けるため、抗精神病薬が1剤になった時点で取りかかる[68]。抗パーキンソン病薬にも副作用と離脱症状があるため、近年では、抗精神病薬の減量か変薬により、抗パーキンソン病薬を極力用いず、そうでなくとも必要最小限にすることが推奨されている[69]。
日本の文献では、一般に精神科病院の入院患者の10〜20%に多飲症が見られ、3〜4%が水中毒を呈していると言われている[70]。
有効性
[編集]定型抗精神病薬の有効性の研究は多数あり、またより新しい非定型抗精神病薬については増加している。
アメリカ精神医学会と英国国立医療技術評価機構は、統合失調症か双極性障害における急性精神病の発現の管理に関して、またさらなる発現の可能性を減少させるための長期間の維持療法に抗精神病薬を推奨している[71][72]。どの抗精神病薬を与えたかで反応は変動するので試行が必要とされ、また低用量が可能であれば推奨されると述べている。多数の研究が、抗精神病薬の投薬計画と「服薬コンプライアンス(遵守)」あるいは「アドヒアランス」の水準に注目し、中止(服薬をやめること)が、患者の入院を含む再発の高い割合に関連していることを明らかにしている。
しかし、統合失調症の診断を受けた人々についての研究で、2009年のシステマティック・レビューとメタアナリシスは、偽薬の24%に比べて、全体の半分以下(41%)しか抗精神病薬に対するなんらかの治療反応を示せないことを見出し、また治療反応は時間と共に減少し、また場合によると試験結果には出版バイアス(試験公開の偏り)があった[73]。さらに、2010年のコクラン共同計画によるリスパダール、最大に販売された抗精神病薬の一つで新世代では最初にジェネリック形式が可能となった、についてのレビューは、偽薬と比較して僅かな恩恵しか見つからず、それにもかかわらず広く用いられ、根拠は限定的なままであり、研究に製薬会社が出資したことに起因するリスパダールの有意にはおそらくバイアスがあり低品質な報告であることを見出した[74]。
2009年の別のコクランのレビューは、双極性障害に関して、第一選択の維持療法として抗精神病薬のオランザピンよりも、従来の気分安定薬であるリチウムのほうが有効性があり、危険性/利益の比率が良好であることを見出した[75]。
うつ病に対する非定型抗精神病薬の有効性についてのメタアナリシスは、効果量が0.34であり、ファンネル・プロットから存在が推測できる出版バイアスの可能性を含めると0.32になり、これはうつ病に対する抗うつ薬の効果量と同じで、統計的には偽薬との差があるが、臨床的に意味のある効果量0.50を下回っていることを見出した[76]。
抗精神病薬の多剤投与(一人の人間に対し同時に2種類以上の抗精神病薬を処方すること)は、日常茶飯事とされているが、必ずしも根拠に基づくか推奨されているものではなく、減少させるよう取り組まれてきた[77]。同様に、過度な高容量(たいてい多剤投与の結果)の継続は、診療ガイドラインおよび、通常はそれ以上効果がなく多くの有害性があると示している根拠に反している[78]。抗精神病薬の薬剤数が増加するほど死亡率も増加する[27]。こういったことに関して現在では過去とは違い、どの量で有効性がどう変わるといった用量依存性や副作用発現率について、また受容体の飽和状態についての論文が増えている。例えば、アリピプラゾール(エビリファイ)の血中濃度が100〜150ng/mLでドーパミンD2およびD3受容体が飽和する[79]。そして、エビリファイの平均投与量が1日に20mgである患者の群の平均血中濃度は228ng/mLと上回っているため、飽和のための血中濃度を上回っている[79]。こうした観察から、抗精神病薬の反応がみられる受容体占有率は65%であり、副作用の可能性が高まるのは高プロラクチン血症では72%、錐体外路作用は78%以上である[12]。
統合失調症に対して、リスペリドン(リスパダール)の最適量はそれ以上では副作用の発現率のみが上昇するため1日4mgである[80]。同様にクエチアピン(セロクエル)では1日300mg[81]、オランザピン(ジプレキサ)では1日10mg[82]である。
アメリカの医療研究・品質調査機構(英語: Agency for Healthcare Research and Quality)によるレビューは、その用途を支持するには科学的な品質が不十分である抗精神病薬の適応外使用(例として、うつ病、認知症、強迫性障害、PTSD、人格障害、トゥレット障害)についての多くの証拠から、特に、脳卒中、振戦、著しい体重増加、鎮静状態、それに胃腸の問題の強い根拠があったことを見出した[83]。イギリスでの子供と青年への認可されていない用法についてのレビューは、見解と懸念が交錯したのに近い報告をした[84]。
知的障害の成人の好戦的で積極的な行動は、元となる根拠が不足しているにもかかわらず、頻繁に抗精神病薬で治療される。一方、最近のランダム化比較試験は偽薬を超える恩恵がないことを見出し、またこのような抗精神病薬の使用は、容認可能な所定の治療とは見なすべきではないことを推奨した[85]。
2006年のコクラン共同計画による、高齢の認知症に対する抗精神病薬の対照試験のレビューは、薬のうち一つか二つは、偽薬と比較して攻撃性や精神病の管理に控え目な恩恵を示したが、これは重篤な有害事象の有意な増加を兼ねていたことを報告した。それは抗精神病薬は、認知症患者の攻撃性や精神病の治療に日課的に使うべきではないが、重度の苦痛あるいは他者への身体的危害の危険性がある少数の事例では選択される可能性があると結論した[86]。
アメリカ国立精神衛生研究所(NIMH)が支援した高齢者の精神障害に対する抗精神病薬の試験がある[87]。ランダム化して4つの非定型抗精神病薬(アリピプラゾール、オランザピン、クエチアピン、リスパダール)を、統合失調症、気分障害、心的外傷後ストレス障害、認知症に対して割り当て、2年間の期間で実施した。結果、疾患と薬剤にかかわらず、中央値26週間の高い中止率や、病理の改善不足が見出され、代謝マーカー(BMI、血圧、血糖値、コレステロール、トリグリセド)が悪化し36.5%がメタボリックシンドロームとなり、危険性/利益の比率がよくないので薬物療法をしない選択も含めよく相談されるべきであるとされた[88]。
いくつかの疑惑が長期間の統合失調症のための抗精神病薬の有効性に関して浮上しており、その一つには2つの大規模な国際的な世界保健機関の研究が見出した、先進国よりも発展途上国(抗精神病薬の入手可能性と使用が少なく、精神福祉の問題はより非公式な地域的な指導による手法だけで治療される)でのほうが、統合失調症と診断された人の長期間の予後が良好という傾向があるという理由がある[89][90]。
ある主張によれば、抗精神病薬が脳を感作しているために、中止すれば精神病を誘発する可能性があることを考慮せずに、当初の症状の再発だと誤って解釈されているという理由で、抗精神病薬の中止・再発の研究に関する根拠には欠陥の可能性がある[91]。対照試験からの根拠は、少なくとも一部の抗精神病薬の服用なしで精神病から回復した統合失調症の人は、抗精神病薬を服用するよりも長期的には良好だろうということを示している[92]。ほかの主張は、全体的に根拠は、抗精神病薬が選択的に用いられ、可能な限り速やかに、徐々に中止した場合にだけ助けになることを示唆しており[93]、さらには「抗精神病薬に関する神話(Myth of the antipsychotic)」[94]が言及している。
抗精神病薬に関する試験で用いられる手法のレビューは、全体的な質は「かなり良い」としているが、参加者の選定の問題を報告している。(統合失調症の試験では、人々の最高90%が対象と排除の詳細な基準を通常適切に満たしておらず、さらに企業の新しい抗精神病薬のマーケティングにもかかわらず、陰性症状は適切に査定されてきていないということを含む);試験の設計の問題(製薬会社は多くのそうしたものに出資し、不適切に試験用の「盲検化」がなされ、試験の参加者は時として偽薬かそうでないかを伝えることができるということを含む);ならびに予後の評価の問題(「反応」を示すスコアの簡略化、回復やクオリティ・オブ・ライフの評価の欠如、高い中断率、公表文献の要約における好都合な結果の選択的な強調、低品質な副作用の報告を含む)[95]。
2013年には、統合失調症を抗精神病薬によって治療した後、薬を減量したグループと中止したグループに分け7年追跡したランダム化比較試験が公開され、中止群は半年での再発率は高いが7年後では同じであり、中止群のほうが有職率が2倍であった[5][96]。
定型対非定型
[編集]以前の定型抗精神病薬と、新世代の非定型抗精神病薬が差別化されるが、大規模試験は統合失調症に対しての有効性や[97]副作用である錐体外路症状の発現率に[98][99]大きな違いがないことを示している。非定型の抗精神病薬は、大脳辺縁系に集中して作用するために錐体外路症状が少ないとされていたが、そのような特性は観察されていない[100]。うつ病に対しては、抗うつ薬と同じで、見出された偽薬に対する有効性の統計的な差は臨床的に無意味な差である[76]。
非定型(第二世代の)抗精神病薬は、定型薬よりも副作用が少なく(特に錐体外路症状)精神病性の症状を回復させるさらなる効果を売りにして販売されており、その効果を示す結果はたびたび頑健性の欠如を示し、そしてその前提には次第に疑問が投げられてきており、それにもかかわらず非定型薬の処方は急上昇してきた[101]。あるレビューはそれらには違いがないと結論し[102]、一方では[103]、非定型のものの「若干大きい有効性」を見出している[102]。しかし、これらの結論を別のレビューが、クロザピン、アミスルピリド、オランザピンとリスペンドンでは、どれがより有効かを明らかにするために問いかけた[102][104]。クロザピンはほかの非定型抗精神病薬よりも有効に見えたが[102][105]、致死的な副作用の可能性が原因で以前には禁止されていた。非定型薬の対照臨床試験は、錐体外路症状を患者の5-15%に生じさせることを報告しているが、実社会の臨床現場における双極性障害の研究では63%の割合で見られ、研究の般化に疑問がもたれる[106]。
2005年にアメリカ政府機関のアメリカ国立精神衛生研究所(NIMH)は、大規模な独立した(製薬会社が出資していない)複数地点の二重盲検試験(CATIE計画)の結果を公表した[107]。同研究は、1,943人の統合失調症の人々で、数種類の非定型抗精神病薬を、古い定型の抗精神病薬のペルフェナジンと比較した。同研究は、中止率(人々が効果を原因として服用をやめた比率)ではオランザピンだけがペルフェナジンより優れていることを見出した。著者は、精神病理と入院率の減少の面で、他の薬に対するオランザピンの有効性が明白に優れていると述べたが、オランザピンは大幅な体重増加の問題(18か月で平均20キログラム)や血糖、コレステロールまたトリグリセドの増加などの比較的重篤な代謝作用に関係していた。使用されたオランザピンの平均と最大投与量は標準的な手法よりもかなり高かったので、このことが、投与量が臨床的に関連のある手法にもっと一致していたほかの調査された非定型抗精神病薬以上の、オランザピンの優れた有効性を説明する偏りの要因として仮定されていた[108]。他の非定型薬の研究(リスパダールとクエチアピン、ジプラシドン)では、尺度を用いて定型のペルフェナジンよりも良好ではなかったし、さらに定型抗精神病薬のペルフェナジンよりも引き起こされた副作用が少ないわけでもなかったが(結果はランセットに発表されたDr.Leuchtによるメタ分析[109]に支持される)、非定型薬剤に比較して多くの患者が錐体外路作用のせいでペルフェナジンを中止した(8% vs. 2% to 4%, P=0.002)。
このCATIE研究のフェーズIIでおおむねそのような研究結果が再現された[110]。このフェーズは、最初のフェーズで薬の服薬を中止した患者の2回目の無作為化である。再びオランザピンだけが結果の評価において目立つ薬だったが、結果は検出力の減少もあり常に統計的有意性に達しなかった(信頼できる発見ではないことを意味する)。非定型薬の投与量が増えたため錐体外路作用には違いがなく、どちらの種類の抗精神病薬でも高用量が錐体外路症状の比率を挙げる要因となっていることが示唆された[99]。次のフェーズ[111]では、ほかの神経弛緩薬よりも投薬における脱落の減少に効果があるクロザピンを臨床医が試すことが認められた。しかし、クロザピンは無顆粒球症を含む中毒性副作用を生じる可能性があり有用性が限定される。
非定型の抗精神病薬への患者のアドヒアランスが高くなるように期待されたが、2008年のレビューは、新規の抗精神病薬の使用が、改善された投薬コンプライアンスおよび良好な臨床的な成果を導くという考えを、データによって立証することができなかったことを明らかにした[112]。
全体的にCATIEと他の研究の評価は、定型薬よりも非定型薬を第一選択とする処方への疑問、さらには2種類の区別への疑問に多くの研究者を導いた[113][114]。対照的に、ほかの研究者は定型薬の遅発性ジスキネジアと錐体外路症状の著しく高い危険性を指摘し、この理由のためだけに非定型薬による治療を第一選択に推奨しているにもかかわらず、後者には代謝性副作用の重大な傾向がある[115]。NICEは最近、非定型薬を優遇するその推奨を改訂し、患者による選択の上で、個々の薬についての特有の特徴に基づいて、個別に選択すべきであることを勧告している[116]。
こうして2009年には、NIMH所長のトーマス・インセルは、以下のような表を示し、「抗精神病薬に関して、現在4つの大規模研究が第一世代の化合物を上回る第二世代の化合物の優位性が乏しいことを証明している[97]」と述べざるを得なかった。
| 研究名 | 治療法 | 設計 | 結果 |
|---|---|---|---|
| Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE) | オランザピン、ペルフェナジン、クエチアピン、リスペリドン、ジプラシドン | 1,943人の統合失調症の患者に1種類の薬物療法を無作為に割り付けた。 | 治療条件の間で症状の改善に違いがないことが観察された;副作用と中止率の違いが薬物療法をまたいで観察された;オランザピンは中止の割合が最も低いことを実証したが、体重増加に関連していた。 |
| Department of Veterans Affairs Cooperative Study Group on the Cost-Effectiveness of Olanzapine | オランザピンかハロペリドール | 309人の統合失調症か統合失調性感情障害の患者に1種類の薬物療法を無作為に割り付けた。 | オランザピンとハロペリドールは、コンプライアンス、症状、錐体外路症状、全体的なクオリティ・オブ・ライフにおける有効性が等しかった;オランザピンは体重増加と高額な費用に関連していた。 |
| Cost Utility of the Latest Antipsychotic Drugs in Schizophrenia Study (CUtLASS 1) | 第一世代と第二世代の抗精神病薬 | 統合失調症、統合失調性感情障害、妄想性障害の227人の患者に、第一世代か第二世代の抗精神病薬による薬物療法のどちらかを受けるように無作為に割り付けた。 | 第一世代と第二世代の抗精神病薬による薬物治療の間に、クオリティ・オブ・ライフ、症状、関連した費用、看護において違いがないことが見出された。 |
| Treatment of Early-Onset Schizophrenia Spectrum Disorders (TEOSS) study | オランザピン、リスペリドン、モリンドン | 統合失調症、統合失調性感情障害、妄統合失調症様障害の119人の若年者(年齢8〜19歳)に1種類の薬物療法を無作為に割り付けた。 | 治療条件の間で反応率あるいは症状減少の大きさにおいて違いがないことが観察された;オランザピンとリスペリドンは体重増加に関連していた一方、モリンドンの治療はアカシジアの自己申告の数の多さに関連していた。 |
脱落率に関して、CATIE計画では18カ月で、投与を受けた1,432人の患者のうち1,061人と患者の74%が脱落し、服薬中止の理由は効果がないか副作用が原因である[117]。8歳から19歳の早期発症統合失調症のTEOSS計画では、116人のうち54人が維持療法に入り、44週間の治療を終えたのは54人のうちの14人と比率では26%であり、残り74%の服薬中止の主な理由は有害事象15人、効果不十分14人、アドヒアランス不履行8人であった[118]。約1年後である52週間後には、当初の116人のうち12人(9%)だけが当初の治療を継続しており、また全員に体重増加を含む副作用があった[118]。
第一世代と第二世代の抗精神病薬による錐体外路作用の発現率には、差がない[98]。
根拠の再評価は、必ずしも非定型薬の処方の偏りを鈍らせていない[119]。
| 薬剤 | PANSS総合スコア (SMD) | 95%信頼区間 |
|---|---|---|
| クロザピン | -0.88 | -1.03 to -0.73 |
| アミスルピリド(未承認) | -0.66 | -0.78 to -0.53 |
| オランザピン | -0.59 | -0.65 to -0.53 |
| リスペリドン | -0.56 | -0.63 to -0.50 |
| パリペリドン | -0.50 | -0.60 to -0.39 |
| ゾテピン | -0.49 | |
| ハロペリドール | -0.45 | |
| クエチアピン | -0.44 | |
| アリピプラゾール | -0.43 | |
| セルチンドール(未承認) | -0.39 | |
| ジプラシドン(未承認) | -0.39 | |
| クロルプロマジン | -0.38 | |
| アセナピン | -0.38 | |
| ルラシドン(未承認) | -0.33 | |
| イロペリドン(未承認) | -0.33 |
分類
[編集]定型抗精神病薬
[編集]定型抗精神病薬(Typical antipsychotic)の治療効果と主要な副作用である錐体外路兆候はドーパミンD2受容体の薬物親和性に相関することが分かっている。定型抗精神病薬のドーパミンD2受容体遮断作用は中枢神経のドーパミン経路すべてに及ぶが、中脳辺縁系(腹側被蓋野から側坐核と腹側線条体、扁桃体と海馬の一部、その他の辺縁系構成部位に投射する。報酬経路をつくることで有名)とおそらく中脳皮質系(腹側被蓋野から大脳皮質特に前頭前野に投射する。これは注意、計画、動機に関与する)への拮抗作用が主要な薬理作用と考えられている。中脳辺縁系の遮断作用が統合失調症の陽性症状の改善に効果がある。また黒質線条体路や下垂体のドーパミンD2受容体の遮断によって薬剤性パーキンソニズムなどの副作用が生じる。陰性症状の改善はセロトニン系の関与などが示唆されており定型抗精神病薬では改善が乏しい傾向にある。非定型抗精神病薬は定型精神病薬と比較してドーパミンD2受容体への作用が緩和されており、セロトニン受容体やドーパミンD4受容体、ドーパミンD2受容体の解離速度などの差からより高い抗精神病作用をもち、錐体外路障害、高プロラクチン血症、心血管系副作用も少ない。定型抗精神病薬の使い方としては非定型抗精神病薬に比べて鎮静作用が強いことからせん妄、不穏の治療や非定型抗精神病薬で治療が無効であった場合が多い。定型抗精神病薬は高力価抗精神病薬と低力価抗精神病薬に大別される。力価は抗精神病作用の強さであり高力価抗精神病薬とはハロペリドールに代表されるブチロフェノン系が中心であり、低力価抗精神病薬はクロルプロマジンに代表されるフェノチアジン系が中心となる。高力価薬は低力価薬に比べて鎮静作用と起立性低血圧の副作用が少なく、低力価薬は高力価薬に比べて錐体外路兆候が少ない傾向になる。これはドーパミンD2受容体との親和性に関係すると考えられている。高力価薬はドーパミンD2受容体への選択性が極めて高いため錐体外路兆候が出やすく、低力価薬はドーパミンD2受容体選択性が低く、ムスカリン受容体やアドレナリンのα受容体へも非特異的な結合を起こし抗コリン作用や抗アドレナリン作用を起こしやすいと考えられている。
フェノチアジン系
[編集]1952年(昭和27年)にはじめて用いられた最初の抗精神病薬であるクロルプロマジンを含む、フェノチアジンを基本骨格とした群である。代表的な薬物としてはクロルプロマジン(商品名:コントミン、ウインタミン)、レボメプロマジン(商品名:ヒルナミン、レボトミン)、チオリダジン(商品名:メレリル)、フルフェナジン(商品名:フルメジン、デポ剤としてフルデカシン)、プロペリシアジン(商品名:アパミン、ニューレプチル)、ペルフェナジン(商品名:ピーゼットシー、トリラホン、トリオミン)などがあげられる。側鎖によって細分類されることがある。クロルプロマジンより強い抗精神病薬としてハロペリドールがある。
- アルキルアミノ側鎖群
クロルプロマジン(商品名:コントミン、ウインタミン)、レボメプロマジン(商品名:ヒルナミン、レボトミン)などが含まれる群である。この群に含まれる薬物はα1遮断作用が強く鎮静作用、催眠作用が非常に強いため興奮、不穏の患者に用いられ、不眠の強い患者の睡眠薬としても用いられる[1]。吐き気止めとしての作用も強いものが多い。非特異的受容体結合も強いため、抗コリン作用も出やすい。低力価抗精神病薬の代表であり、一日200mg程度の使用が一般的である[1]。
- ピペリジン側鎖群
プロペリシアジン(商品名:アパミン、ニューレプチル)などが含まれる。低力価抗精神病薬のなかでは力価は強い。錐体外路障害が弱く、抗コリン作用、起立性低血圧が多いのは他の低力価抗精神病薬と同様である。α1遮断作用は強いが悪心に対しては効果が弱い。
- ピペラジン側鎖群
フルフェナジン(商品名:フルメジン、デポ剤としてフルデカシン)、ペルフェナジン(商品名:ピーゼットシー)などが含まれる。鎮吐作用が強いものが多く周術期の鎮吐薬としてよく用いられる。他のフェノチアジン系に比べるとかなり高力価であり高力価抗精神病薬としての特性をもつ。
ブチロフェノン系
[編集]定型抗精神病薬の代表的系列である。これはハロペリドール(商品名:セレネース、ハロステン、デポ剤としてハロマンスなど)が含まれるからである。高力価抗精神病薬の代表格でもある。抗コリン作用は弱く、錐体外路障害は起こりやすい[1]、α1遮断作用は弱いが鎮吐作用は強い。代表的な薬物としてはハロペリドール(商品名:セレネース、ハロステン、デポ剤としてハロマンスなど)、ブロムペリドール(商品名:インプロメン)、チミペロン(商品名:トロペロン)、スピペロン (商品名:スピロピタン)、ピモジド(商品名:オーラップ)
ベンズアミド系
[編集]鎮吐薬であったドーパミン拮抗薬であるメトクロプラミドを改良する過程で生じた系列である。スルピリド(商品名:ドグマチール、アビリット、ミラドールなど)、スルトプリド(商品名:バルネチール)、ネモナプリド(商品名:エミレース)などが知られている。ドーパミン受容体の中でドーパミンD1受容体の阻害作用が殆どない系列である。スルピリドはドーパミンD3受容体を強く抑制し覚醒度を低下させず、精神活動抑制作用が殆どなく、錐体外路障害も極めて稀である。幻覚や妄想を抑制する効果はかなり高い。脱抑制作用も強い。消化管と中枢神経の両方に効果があるためストレス性胃潰瘍などには非常に良い効果がある。うつ病や神経症にもよく用いられる。スルトプリドは全く毛色が異なり強力な鎮静作用をもち、錐体外路障害が強い。躁病の治療に用いられることがある。ネモナプリドはドーパミンD2受容体、ドーパミンD3受容体、ドーパミンD4受容体を抑制しかなり強力な抗幻覚、抗妄想作用をもち、副作用も弱い。
インドール系
[編集]オキシペルチンが含まれる。
その他
[編集]ゾテピン(商品名:ロドピン)en:Zotepine、モサプラミン(商品名:クレミン)、クロカプラミン(商品名:クロフェクトン)など。
非定型抗精神病薬
[編集]非定型抗精神病薬(Atypical antipsychotic)は定型抗精神病薬と比較してドーパミンD2受容体への作用が緩和されており、セロトニン受容体やドーパミンD4受容体、ドーパミンD2受容体の解離速度などの差からより高い抗精神病作用をもち、錐体外路障害、高プロラクチン血症、心血管系副作用も少ない。しかし、アリピプラゾールの使用で約半数の者に低プロラクチン血症が起こる[121]。リスパダールは、強力なドーパミン遮断作用があり、定型抗精神病薬であるセレネースと同等の抗幻覚作用を発揮する。リスパダールは、コントミンのドーパミン遮断作用を勝るものである。

- 日本で処方可能なもの
- 日本ではまだ承認されていないもの。(新薬承認の遅延については、ドラッグ・ラグを参照のこと)
セロトニン・ドーパミン拮抗薬
[編集]セロトニン・ドーパミン拮抗薬(serotonin-dopamine antagonist, SDA)は、リスペリドン(商品名:リスパダール)、ペロスピロン(商品名:ルーラン)、ブロナンセリン(商品名:ロナセン)、ジプラシドンen:Ziprasidone、セルチンドールen:Sertindole、オランザピン(商品名:ジプレキサ)、クエチアピン(商品名:セロクエル)が含まれる系列である。クエチアピン(商品名:セロクエル)は他の受容体にも関与するため毛色が異なる。典型的なSDAとしてはリスペリドン(商品名:リスパダール)と考えられる。5-HT系がドーパミン機能を抑制し、5-HT拮抗によりドーパミン系が脱抑制されるために錐体外路障害が軽減すると考えられている。陰性症状の改善は前頭葉皮質におけるドーパミン系脱抑制の結果とも考えられているがコンセンサスを得られていない。ペロスピロン(商品名:ルーラン)はアザピロン系誘導体の抗不安薬の仲間であり、5-HT1A受容体のパーシャルアゴニストの側鎖を改良することで抗ドーパミン作用を有するようになった。ブロナンセリン(商品名:ロナセン)は新しいSDAであり、リスペリドンと同様の抗精神病作用をもち、副作用が軽減すると考えられている。
ジベンゾチアゼピン系
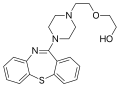
[編集]SDAに分類されるクエチアピン(商品名:セロクエル)は他のSDAと異なる。ドーパミンD2受容体に比べて5-HT2受容体に対する親和性が高く、5-HT1受容体、アドレナリンα1、α2、ドーパミンD1受容体などに弱い親和性を持ち、ムスカリン受容体、ベンゾジアゼピン受容体には殆ど親和性がない。
せん妄や難治性の不眠症に対して低用量で用いられる。また難治性の統合失調症でも用いられる。
多元受容体標的化抗精神病薬
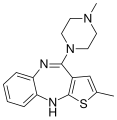
[編集]多元受容体標的化抗精神病薬(multi-acting-receptor-targeted-antipsychotics, MARTA)は、オランザピン(商品名:ジプレキサ)が含まれる。ドーパミンD2受容体群(D2、D3、D4)、5-HT2受容体、5-HT6受容体、アドレナリンα1、ヒスタミンH1受容体に高い親和性を持っている。ムスカリン受容体の親和性は生体内では低い。
ドーパミン系安定剤
[編集]ドーパミン系安定剤(Dopamine System Stabilizer, DSS)は、アリピプラゾール(商品名:エビリファイ)が含まれる新しい非定型抗精神病薬である。ドーパミンD2受容体のパーシャルアゴニスト、5-HT1A受容体のパーシャルアゴニストであり、5-HT2A受容体のアンタゴニストである。パーシャルアゴニストによる安定化作用により副作用が出にくいとされている。しかし、実際は”ギャンブル・食事・ショッピング・セックス”への抑えがたい衝動と、他人への危害についてアメリカ食品医薬品局 (FDA) が警告している[122]。アリピプラゾールは抗精神病薬の中で最も暴力の報告が多かった(p<0.001)[123]。低プロラクチン血症も約半数の者に起こる[121]。解離性麻酔薬のフェンサイクリジン(PCP)もD2受容体パーシャルアゴニストであるが、アリピプラゾールよりは結合親和性が低い[124][125]。
作用機序
[編集]複数のニューロンが神経系の機能単位を形成する構築様式は長経路型、局所回路型、単一源発散型の3つのパターンしか存在しない。末梢神経は長経路型のみが利用され、中枢神経では3つの様式が全て用いられる。
- 長経路型
末梢神経の感覚や運動の経路などが非常に有名である。運動器や末梢受容体と中枢神経を比較的単純な神経回路で結び、情報の統合や修飾は極めて少ない。自律神経の場合はひとつの節前線維が複数の節後線維と連絡をつくり発散型のシグナル伝達をとる。発散型のシグナル伝達では情報の加工や修飾が加わることが多いが、自律神経系の場合はそのようなことはない。中枢神経での長経路型のニューロンは情報の統合や修飾を行う。上流から多数の連絡を受け収束型のシグナル伝達をしながら、下流へも多数の連絡があり、発散型のシグナル伝達を行う。このため中心周辺型のシグナル伝達とも言われる。視床の感覚ニューロンは末梢から全身からの感覚情報を受けて、中心後回の特定の部位のみを興奮させ、さらにその周辺部位を抑制する作用をもつ。
- 局所回路型
局所回路型では主に隣接する領域内部のニューロン連絡を維持し、一般にシグナル伝達の調節に関与する。大脳皮質に非常に多く存在する回路である。外側膝状体では特定の発火パターンに対応して皮質領域を興奮させる回路がある。これによって直線を見たとき、直線を認識する皮質領域が興奮し、直線と認知ができると考えられている。
- 単一発散型
脳幹、視床下部、前脳基底部に存在する神経核では単一の神経核に起始する複数のニューロンが多数の標的細胞を神経支配し、単一源発散型の神経回路を構築する。広範系の構築ともいう。主にG蛋白共役型受容体に作用する生体アミンを利用して調節的に影響する場合が多い。
| 起始 | 神経伝達物質 | 機能 |
|---|---|---|
| 中脳黒質 | ドーパミン | 目的ある運動、感情、思考、記憶蓄積 |
| 橋青斑核 | ノルアドレナリン | 覚醒や不意の刺激への応答 |
| 脳幹縫線核 | セロトニン | 痛覚、気分、大脳皮質の応答性 |
| マイネルト基底核 | アセチルコリン | 覚醒 |
| 脚橋被蓋核 | アセチルコリン | 睡眠覚醒周期 |
| 視床下部隆起乳頭体核 | ヒスタミン | 前脳の賦活作用 |
多くの向精神薬が非特異的な受容体結合にて薬理活性を持つため、広範系が関与すると思われる数多くの薬理作用が認められる。近年多くの抗精神病薬が気分に関与すると考えられているセロトニン、ノルアドレナリンへの影響が認められるためかつては抗精神病薬は統合失調症治療薬としての側面が強調されていたがうつ病、神経症といった数多くの疾患に用いられる傾向がある。また単一発散型の神経回路に作用する薬物以外に中枢神経細胞の活動を直接変化させる薬物療法も存在する。中枢神経系では興奮アミノ酸であるグルタミン酸、抑制アミノ酸であるγ-アミノ酪酸 (GABA) が有名である。GABA受容体に作用する薬物として抗てんかん薬や抗不安薬(多くはベンゾジアゼピン系)も併用することがある。またNaチャネルに作用する抗てんかん薬としてフェニトイン(商品名アレビアチン)やバルプロ酸(商品名デパケン)、カルバマゼピン(商品名テグレトール)T型カルシムチャネルに作用する薬物としてバルプロ酸(商品名デパケン)も併用されることがある。
ハロペリドールはNMDA受容体アンタゴニストとして作用する。IC50は2µMであり最大80%阻害する[126]。
歴史
[編集]1856年にイギリスの化学者ウィリアム・パーキンが、コールタールから得られるフェノチアジンに似た化合物が染料として用いることができることを発見した[127]。
合成染料のフェノチアジン系のメチレンブルーから[128]、ローヌ・プーラン社がRP4560、後に抗精神病薬のクロルプロマジンと呼ばれることになる化合物を合成した[127]。
抗精神病薬は遅発性ジスキネジアを引き起こすため、1974年に訴訟が起こり、しばらく新しい抗精神病薬は市場に出なくなった[129]。抗精神病薬のクロザピンには致命的な副作用があったが、遅発性ジスキネジアがないためクロザピンの受容体結合特性を模倣したリスペリドン(リスパダール)、ジプラシドン、クロザピンの分子構造を若干修正したクエチアピン(セロクエル)、オランザピン(ジプレキサ)が合成され、90年代以降に市場に出ることになる[129]。
2010年ころから製薬会社は、既存の薬の構造を少し修正し特許を取得した模倣薬(me too drug)を販売するという手法ではすでに収益の見込みがないとみて、グラクソ・スミスクライン、アストラゼネカ、メルクなどの大手製薬会社が精神科領域の薬の開発から撤退しはじめた[130]。
社会的側面
[編集]売上高
[編集]抗精神病薬は2008年に世界中で220億ドルの利益を出し、全医薬品中で一番売れており最も利益がある[131]。アメリカで2003年に、推定321万人の患者が抗精神病薬を受け取り、これは推定28.2億ドルに相当する。処方箋の3分の2以上が、新しい高価な非定型の薬であり、平均164ドルの原価計算になるのに比べて、古い薬では40ドルであった[132]。2008年のアメリカでの販売利益は146億ドルに達し、アメリカの治療分野で最大に販売される薬である[133]。
議論
[編集]『ガーディアン』に言わせると:「精神医学に反対する意見の長年にわたる核心は、昔から苦悩の治療に薬が、特に抗精神病薬が用いられてきたことである。これらの薬は実のところどんな「精神状態」をねらいにしている?すなわち、化学的な管理—妄想症、欺まん、困窮、奇妙さ、それに風変わりを社会的に有益になるように減らすために、半植物人間にすることか?」[94]
介護施設におけるこの種類の薬の使用は批判の歴史を持つ。批判する人々は、患者を穏やかでより従順にするために薬を使い過ぎると主張する。外部の医師は介護施設のスタッフからのプレッシャーを感じている[134]。イギリス政府の大臣らに委託された非公式の調査は、認知症介護における抗精神病の医薬品の不必要な使用がまん延し、年間1800人の死亡に結びついていたことを報告した[135][136]。アメリカ政府は、老人ホームでの抗精神病薬のリスパダールの販売促進に対して、製薬会社ジョンソン・エンド・ジョンソンがオムニケアに手数料を支払った容疑で法的措置を開始した[137]。
統合失調症の維持療法には反論がある[59][138]。維持療法に関する研究のレビューは、長期間の抗精神病薬治療は偽薬よりも統合失調症の患者の再発を減少させるのに優れていると結論しているが、研究の一部は小規模である[139]。北米における大規模な横断研究のレビューでは、適度な数の統合失調症の患者が症状から自然に回復したように見え、一部の患者は維持投薬の必要はなかった可能性が高いことを明らかにした[138]。また、長期的な抗精神病薬による維持管理の多くの研究には、再発率に対する抗精神病薬の離脱症状の役割を考慮しなかったことに起因する欠陥がある可能性があると論じられている[59]。
また論争は、製薬会社による副作用の軽視あるいは隠ぺいの疑惑、条件の拡大あるいは適応外使用の違法な販売促進を含めた、抗精神病薬のマーケティングと販売促進の役割に関している;影響する臨床試験(あるいはそれらの出版)は、高額で利益が多い新しい非定型薬が、特許が切れた古い安価な定型薬よりもすぐれていたことを示すのを試みている。違法マーケティングの告発を受けての、2つの大きな製薬会社による支払いは、法人に課された最大の刑事上の罰金としてアメリカ史上記録的となった[140]。ある事例は、イーライリリー・アンド・カンパニーの非定型抗精神病薬のジプレキサが関与し、ほかの事例はベクストラが関与した。ベクストラの例では、政府は、他の抗精神病薬のジプラシドンの違法マーケティングでファイザーを起訴した[140]。その上、アストラゼネカは、販売活動についての連邦政府による捜査中に、セロクエル(クエチアピン)の元使用者からの非常に多くの人身傷害の訴訟に面した[141]。 それが示唆する状況を展開すると、アストラゼネカのセロクエルとイーライリリーのジプレキサは、2008年に世界的な販売額でそれぞれ55億円と54億円と、抗精神病薬を最大に販売している[131]。
ハーバード大学医学部教授のジョセフ・ビーダーマンは、子供の双極性障害の診断が増加していることに関する調査を行った。2008年の議会による調査は、ビーダーマンが2000年から2007年の間に、双極性障害の子供に対して処方される抗精神病薬の製造業者を含む企業から、講演とコンサルタントの謝礼として160万ドルを受け取っていたことを明らかにした—その一部はハーバードに未公開であった。ジョンソン・エンド・ジョンソンは、同社の抗精神病薬のリスパダールについての研究も行われていたという、2002年から2005年にかけてビーダーマンが率いた研究施設に70万ドル以上を贈った。ビーダーマンは、お金は自分に影響を与えなかったし、特定の診断や治療を促進していないと返答している[140]。
また一部の批判者らは、精神福祉の課題を決めようと、製薬会社が出資したフロント機関および患者と対立する「弁護」団が申し立てに使われ、それは暴力の危険性についての主張によってしばしば正当化され、人々の希望に反して抗精神病薬を投与するために法律を強いることを含んでいると分析している[142]。
訴訟
[編集]ジプレキサ(オランザピン)は1996年に市場に出たが、服用後に糖尿病やほかの病気になったとの訴えがあり、2005年には8,000件の訴訟に対して7億ドル、2007年には18,000件の訴訟に対して5億ドル支払っている[143]。
各製薬会社は、適応外使用を勧める違法なマーケティングで、史上最高額の罰金を更新し続けている[13]。多くは、死亡リスクを高めるという証拠があるのにかかわらず高齢者に販売促進したことや、適応外の小児へ、あるいは統合失調症や双極性障害以外の承認されていない用途の違法なマーケティングによる。
2006年、アラスカ州最高裁判所は抗精神病薬に関する訴訟の判決文で、「向精神薬は患者の心身に重大で永続的な悪影響を及ぼすことがある[注釈 2]」「数々の破壊的な副作用を引き起こす可能性があることが知られている[注釈 3]」と説明している[144]。
2007年には、ブリストル・マイヤーズ スクイブは、非定型抗精神病薬エビリファイ(アリピプラゾール)の、承認されていない小児への使用と、認知症の高齢者では致命的な副作用があるという黒枠警告を考慮しない違法なマーケティングにより、5.15億ドルの罰金が科された[13][148]。
2009年、イーライリリーは、非定型抗精神病薬ジプレキサ(オランザピン)を、体重増加などの副作用の情報を告知せず、また常用量で死亡リスクを高める老人への睡眠薬としての利用を勧める「午後5時に5mg」などの違法なマーケティングにより14億ドルの罰金が科された[13][149]。
2009年、ファイザー、ジプラシドンの適用外用途のマーケティングにより、3.01億ドルの罰金が科された[150]。
2010年、アストラゼネカは、非定型抗精神病薬セロクエル(クエチアピン)を高齢者や、死亡リスクを高める小児に適応外の違法なマーケティングを行い5.2億ドルの罰金が科された[13][151]。
2012年、ジョンソン・エンド・ジョンソンは、非定型抗精神病薬リスパダール(リスペリドン)の小児や高齢者への適応外のマーケティングや、薬が体重増加や糖尿病と相関するというデータの隠ぺい、またほかの薬の違法なマーケティングにより係争中であり、15〜20億ドルが科されるとみられている[13]。リスパダールを処方するごとに5,000ドルの罰金で係争中である[152]。
抗精神病作用が報告されている物質
[編集]あるレビューでは、大麻の成分であるカンナビジオール (CBD) は、抗精神病薬の特性が報告されており、統合失調症の患者への臨床試験は複数行われているが、42人の被験者を用いた試験では4週間でアミスルプリドに匹敵する有効性があり、CBDでは、体重増加、錐体外路症状、プロラクチン増加がなく副作用の点で優れていた。一方28人を対象とした急性投与(単回投与)では効果を示さないため、著者は4週間のうちに抗精神病特性を発揮すると思われると付記している。なおこちらでも副作用の報告がない[153]。2017年時点で、オランダでエコー製薬による、Arvisolという経口錠剤の治験第I相(初期段階を意味する)が進行しており、対象はてんかんと統合失調症である[154]。2012年8月に報告された6件のシステマティックレビューを再分析したメタアナリシスにおいて、GRADEアプローチを使用した結果表が示され、発見された2件のランダム化試験はメタアナリシスに組み込むことができなかったため、文章的な情報を統合し、大麻の成分であるカンナビジオール(CBD)は統合失調症の症状を改善せず、頻繁な副作用を引き起こすと結論付けら、その証拠の確実性は中等度とされる[155]。このレビューで発見された2つのランダム化比較試験は[155]、出典をさかのぼると(先に言及したものと違う媒体で発表され結論が同様の)42人の被験者でアミスルピリドと比較した4週間の試験と、(先に言及したものと同一の)28人への単回投与の試験から導き出されている。2017年12月には、多施設88人でのランダム化試験の統合失調症へのCBDの結果が報告され、6週間後には陽性症状(幻覚・妄想)が少なく、またドーパミン受容体への拮抗作用ではないため、新しい治療法である可能性を示した[156]。
多価不飽和脂肪酸の代謝異常が統合失調症の発症にかかわるのではないかとみられており、ω-3脂肪酸を投与する研究が行われている[157]。
最も一般的なミクログリア抑制剤として知られているテトラサイクリン系抗生物質のミノサイクリンを抗精神病薬と追加・併用することで、統合失調症の陰性症状を特に改善することが、4つのメタアナリシス・システマティックレビューを基にしたメタレビューで示されている[158]。また予防効果として、痤瘡(にきび)治療における長期間のミノサイクリン使用が、他の治療と比較して、その後の統合失調症の診断リスク減少と関連することが示されている[159]。抗生物質の使用は、薬剤耐性菌を生む問題があり感染症においても適正使用が言われており、感染症でもない状況での抗生物質の不適切使用は戒められる[160]。
脚注
[編集]注釈
[編集]- ^ 抗精神病薬は、通常、向精神薬のカテゴリに含まれる薬剤として扱われる。(参考:厚生労働省平成22年9月10日障精発0910第1号「向精神薬等の過量服薬への取組について」においての「向精神薬(抗うつ薬、抗不安薬、睡眠薬、抗精神病薬)」の記述など (参照(厚生労働省法令データベースサービス)))
- ^ 原文: “psychotropic medication can have profound and lasting negative effects on a patient's mind and body” [144][145][146][147]
- ^ 原文: “are known to cause a number of potentially devastating side effects.” [144][145][146][147]
出典
[編集]- ^ a b c d e f g h i j k l m 世界保健機関 2010, PSY.
- ^ a b 世界保健機関 2010, BPD.
- ^ a b c d e アメリカ精神医学会『DSM-5 精神疾患の診断・統計マニュアル』日本精神神経学会日本語版用語監修・高橋三郎・大野裕監訳・染矢俊幸・神庭重信・尾崎紀夫・三村將・村井俊哉訳、医学書院、2014年6月30日、703-707頁。ISBN 978-4260019071。
- ^ Mitchell, A. J.; Delaffon, V.; Vancampfort, D.; Correll, C. U.; De Hert, M. (January 2011). “Guideline concordant monitoring of metabolic risk in people treated with antipsychotic medication: systematic review and meta-analysis of screening practices”. Psychological Medicine 42 (01): 125–147. doi:10.1017/S003329171100105X. PMID 21846426.
- ^ a b Wunderink, Lex; Nieboer, Roeline M.; Wiersma, Durk; Sytema, Sjoerd; Nienhuis, Fokko J. (September 2013). “Recovery in Remitted First-Episode Psychosis at 7 Years of Follow-up of an Early Dose Reduction/Discontinuation or Maintenance Treatment Strategy” (pdf). JAMA Psychiatry 70 (9): 913. doi:10.1001/jamapsychiatry.2013.19. PMID 23824214.
- ^ 厚生労働省『精神科医療について』(pdf)(プレスリリース)2011年11月2日、111-113頁。2013年7月11日閲覧。
- ^ 厚生労働省自殺・うつ病等対策プロジェクトチーム『過量服薬への取組-薬物治療のみに頼らない診療体制の構築に向けて』(pdf)(プレスリリース)2010年9月9日、7-8頁。2013年3月15日閲覧。
- ^ 『抗精神病薬減量法ガイドラインを発表 -多剤大量処方から少しずつ最適な処方への工夫』(プレスリリース)独立行政法人国立精神・神経医療研究センター、2013年10月4日。
- ^ a b 田辺英 著「60 抗精神病薬の離脱症状について教えてください。」、藤井康男(編集)、稲垣中(編集協力) 編『統合失調症の薬物療法100のQ&A』星和書店、2008年5月、194-195頁。ISBN 978-4791106677。
- ^ a b Huhtaniska, Sanna; Jääskeläinen, Erika; Hirvonen, Noora; et al. (2017). “Long-term antipsychotic use and brain changes in schizophrenia - a systematic review and meta-analysis”. Human Psychopharmacology: Clinical and Experimental 32 (2): e2574. doi:10.1002/hup.2574. PMID 28370309.
- ^ a b Nordström, Peter; Nordström, Anna; Eriksson, Marie; Wahlund, Lars-Olof; Gustafson, Yngve (September 2013). “Risk Factors in Late Adolescence for Young-Onset Dementia in Men” (pdf). JAMA Internal Medicine 173 (17): 1612. doi:10.1001/jamainternmed.2013.9079. PMID 23939347.
- ^ a b Kapur, S. (April 2000). “Relationship Between Dopamine D2 Occupancy, Clinical Response, and Side Effects: A Double-Blind PET Study of First-Episode Schizophrenia”. American Journal of Psychiatry 157 (4): 514–520. doi:10.1176/appi.ajp.157.4.514. PMID 10739409.。
- ^ a b c d e f Maia Szalavitz Sept (2012年9月17日). “Top 10 Drug Company Settlements”. TIME.com 2013年2月23日閲覧。
- ^ 英国国立医療技術評価機構 2014, Chapt.1.3.4.
- ^ 英国国立医療技術評価機構 2014, Chapt.1.3.2.1.
- ^ 英国国立医療技術評価機構 2014, Chapt.1.2.3.2.
- ^ 英国国立医療技術評価機構 2014b, Chapt.1.10.13.
- ^ a b 英国国立医療技術評価機構 (November 2006). CG42 - Dementia: Supporting people with dementia and their carers in health and social care (Report). Chapt.1.7.
- ^ 王立オーストラリア総合医学会 (2006-03), Medical care of older persons in residential aged care facilities (silver book), The Royal Australian College of General Practitioners, p. 32, ISBN 0-86906-212-3
- ^ アメリカ精神医学会 (September 2013). Five Things Physicians and Patients Should Question. Choosing Wisely (Report). ABIM Foundation.
- ^ QS53 - Anxiety disorders (Report). 英国国立医療技術評価機構. February 2014. Quality statement 3.
- ^ Bellack AS (July 2006). “Scientific and Consumer Models of Recovery in Schizophrenia: Concordance, Contrasts, and Implications”. Schizophrenia Bulletin 32 (3): 432–42. doi:10.1093/schbul/sbj044. PMC 2632241. PMID 16461575.
- ^ Mangrella M, Motola G, Russo F et al. (1998). “[Intensive hospital monitoring of adverse reactions to benzodiazepines and neuroleptic agents]” (Italian). Minerva Medica 89 (7–8): 293–300. PMID 9824992.
- ^ Healy 2009, p42. Psychiatric drugs explained 5th ED. Edinburgh : Elsevier Churchill Livingstone
- ^ Artaloytia, J. F. (March 2006). “Negative Signs and Symptoms Secondary to Antipsychotics: A Double-Blind, Randomized Trial of a Single Dose of Placebo, Haloperidol, and Risperidone in Healthy Volunteers”. American Journal of Psychiatry 163 (3): 488–493. doi:10.1176/appi.ajp.163.3.488. PMID 16513871.
- ^ Weinmann, Stefan; Read, John; Aderhold, Volkmar (August 2009). “Influence of antipsychotics on mortality in schizophrenia: Systematic review”. Schizophrenia Research 113 (1): 1–11. doi:10.1016/j.schres.2009.05.018. PMID 19524406.
- ^ a b Joukamaa, M. (February 2006). “Schizophrenia, neuroleptic medication and mortality”. The British Journal of Psychiatry 188 (2): 122–127. doi:10.1192/bjp.188.2.122. PMID 16449697.
- ^ “Public Health Advisory: Deaths with Antipsychotics in Elderly Patients with Behavioral Disturbances”. FDA (2005年4月11日). 2013年3月20日閲覧。
- ^ a b Glever, J (2008年). “Boxed Mortality Warning Added to Older Antipsychotics Given to Elderly Demented”. Medpage Today 2009年4月24日閲覧。
- ^ Kales, Helen C.; Kim, Hyungjin Myra; Zivin, Kara; Valenstein, Marcia; Seyfried, Lisa S.; Chiang, Claire; Cunningham, Francesca; Schneider, Lon S. et al. (January 2011). “Risk of Mortality Among Individual Antipsychotics in Patients With Dementia”. The American Journal of Psychiatry 169 (1): 71–9. doi:10.1176/appi.ajp.2011.11030347. PMID 22193526.
- ^ Schneider-Thoma J, Efthimiou O, Huhn M, et al. (August 2018). “Second-generation antipsychotic drugs and short-term mortality: a systematic review and meta-analysis of placebo-controlled randomised controlled trials”. Lancet Psychiatry (8): 653–663. doi:10.1016/S2215-0366(18)30177-9. PMID 30042077.
- ^ Fourrier-Réglat, Annie (April 2012). “Antipsychotic Use and Myocardial Infarction in Older Patients With Treated Dementia”. Archives of Internal Medicine 172 (8): 648. doi:10.1001/archinternmed.2012.28. PMID 22450214.
- ^ Trifirò G, Gambassi G, Sen EF, Caputi AP, Bagnardi V, Brea J, Sturkenboom MC (April 2010). “Association of community-acquired pneumonia with antipsychotic drug use in elderly patients: a nested case-control study”. Annals of Internal Medicine 152 (7): 418–25, W139–40. doi:10.1059/0003-4819-152-7-201004060-00006. PMID 20368647.
- ^ a b Schizophrenia Drugs May Spur Subtle Brain Tissue Loss. Drugs.com.
- ^ Ho, Beng; Andreasen, Nancy C.; Ziebell, Stephen; Pierson, Ronald; Magnotta, Vincent (Feb. 2011). “Long-term antipsychotic treatment and brain volumes: a longtitudinal study of first-episode schizophrenia”. Archives of General Psychiatry 68 (2): 128–37. doi:10.1001/archgenpsychiatry.2010.199. PMC 3476840. PMID 21300943 2011年4月5日閲覧。.
- ^ lewis, David A (Feb. 2011). “Antipsychotic medications and brain volume: do we have a cause for concern?”. Archives of General Psychiatry 68 (2): 126–27. doi:10.1001/archgenpsychiatry.2010.187.
- ^ 抗精神病薬による脳への負の影響。その1 灰白質への影響 場末P科病院の精神科医のblog
- ^ 抗精神病薬による脳への負の影響。その2 白質への影響 場末P科病院の精神科医のblog
- ^ Dorph-Petersen, Karl-Anton; Pierri, Joseph N; Perel, James M; Sun, Zhuoxin; Sampson, Allan R; Lewis, David A (2005). “The Influence of Chronic Exposure to Antipsychotic Medications on Brain Size before and after Tissue Fixation: A Comparison of Haloperidol and Olanzapine in Macaque Monkeys”. Neuropsychopharmacology 30 (9): 1649–1661. doi:10.1038/sj.npp.1300710. ISSN 0893-133X.
- ^ Radua, J.; Borgwardt, S.; Crescini, A.; Mataix-Cols, D.; Meyer-Lindenberg, A.; McGuire, P.K.; Fusar-Poli, P. (November 2012). “Multimodal meta-analysis of structural and functional brain changes in first episode psychosis and the effects of antipsychotic medication”. Neuroscience & Biobehavioral Reviews 36 (10): 2325–2333. doi:10.1016/j.neubiorev.2012.07.012. PMID 22910680.
- ^ Zonnenberg C, Bueno-de-Mesquita JM, Ramlal D, Blom JD (2017). “Hypothermia due to Antipsychotic Medication: A Systematic Review”. Front Psychiatry: 165. doi:10.3389/fpsyt.2017.00165. PMC 5594062. PMID 28936184.
- ^ Ruchita Shah; Sandeep Grover; Uma Maheshwari; Natasha Kate; Nidhi Malhotra (2010). “Acute akathisia with quetiapine: A case report and review of literature”. Indian Journal of Pharmacology. PMC 2991706.
- ^ Weston-Green, K; Huang XF, Lian JM, Deng C (May 2012). “Effects of olanzapine on muscarinic M3 receptor binding density in the brain relates to weight gain, plasma insulin and metabolic hormone levels”. European Neuropsychopharmacology 22 (5): 364–73. doi:10.1016/j.euroneuro.2011.09.003. PMID 21982116.
- ^ Ruiz de Azua, I; Gautam D; Guettier JM; Wess J (February 2011). “Novel insights into the function of [beta-cell M3 muscarinic acetylcholine receptors: therapeutic implications”]. Trends in Endocrinology & Metabolism 22 (2): 74–80. doi:10.1016/j.tem.2010.10.004. PMC 3053051. PMID 21106385.
- ^ Torrey EF, Swalwell CI (December 2003). “Fatal olanzapine-induced ketoacidosis”. The American Journal of Psychiatry 160 (12): 2241. doi:10.1176/appi.ajp.160.12.2241. PMID 14638601.
- ^ Koller EA, Doraiswamy PM (July 2002). “Olanzapine-associated diabetes mellitus”. Pharmacotherapy 22 (7): 841–52. doi:10.1592/phco.22.11.841.33629. PMID 12126218.
- ^ Koller EA, Cross JT, Doraiswamy PM, Malozowski SN (September 2003). “Pancreatitis associated with atypical antipsychotics: from the Food and Drug Administration's MedWatch surveillance system and published reports”. Pharmacotherapy 23 (9): 1123–30. doi:10.1592/phco.23.10.1123.32759. PMID 14524644.
- ^ Deng, C; Weston-Green K; Huang XF (2010-02-01). “The role of histaminergic H1 and H3 receptors in food intake: A mechanism for atypical antipsychotic-induced weight gain?”. Progress in Neuro-Psychopharmacology and Biological Psychiatry 34 (1): 1–4. doi:10.1016/j.pnpbp.2009.11.009. PMID 19922755.
- ^ Weston-Green, K; Huang XF, Deng C (2012-03-16). Chang, Alice Y. W. ed. “Alterations to Melanocortinergic, GABAergic and Cannabinoid Neurotransmission Associated with Olanzapine-Induced Weight Gain”. PLoS One 7 (3): e33548. doi:10.1371/journal.pone.0033548. PMC 3306411. PMID 22438946.
- ^ Hasnain M, Vieweg WVR, Fredrickson SK (2010). “Metformin for Atypical Antipsychotic-Induced Weight Gain and Glucose Metabolism Dysregulation: Review of the Literature and Clinical Suggestions”. CNS Drugs 24 (3): 193–206. doi:10.2165/11530130-000000000-00000. PMID 20155995.
- ^ Weston-Green, K; Huang XF, Deng C (February 2010). “Sensitivity of the female rat to olanzapine-induced weight gain--far from the clinic?”. Schizophrenia Research 116 (2–3): 299–300. doi:10.1016/j.schres.2009.09.034. PMID 19840894.
- ^ Baldessarini, Ross J.; Frank I. Tarazi (2006). “Pharmacotherapy of Psychosis and Mania”. In Laurence Brunton, John Lazo, Keith Parker (eds.). Goodman & Gilman's The Pharmacological Basis of Therapeutics (11th ed.). New York: McGraw-Hill. ISBN 978-0-07-142280-2. OCLC 150149056[要ページ番号]
- ^ “FDA Drug Safety Communication: Antipsychotic drug labels updated on use during pregnancy and risk of abnormal muscle movements and withdrawal symptoms in newborns”. FDA (2011年2月22日). 2013年1月27日閲覧。
- ^ 上平忠一「精神分裂病における知覚変容発作の臨床的研究 : 自験例を中心にして」『長野大学紀要』第23巻第1号、長野大学、2001年6月30日、10-21頁、CRID 1050564287518429952、ISSN 0287-5438、NAID 40004066379。
- ^ “Antipsychotic-induced paroxysmal perceptual alteration in a patient with major depressive disorder”. Psychiatry and Clinical Neurosciences 63 (3): 429–430. (June 2009). doi:10.1111/j.1440-1819.2009.01963.x. PMID 19566782.
- ^ Bozkurt, Hasan; Ayaydın, Hamza; Adak, İbrahim; Zoroğlu, S. Salih (December 2012). “Risperidone-Induced Paroxysmal Perceptual Alteration in a Child with Autism”. Journal of Child and Adolescent Psychopharmacology 22 (6): 470–471. doi:10.1089/cap.2012.0053. PMID 23234592.
- ^ 統合失調症の薬物療法100のQ&A 星和書店 p.281
- ^ Dilsaver, SC.; Alessi, NE. (Mar 1988). “Antipsychotic withdrawal symptoms: phenomenology and pathophysiology”. Acta Psychiatr Scand 77 (3): 241–6. doi:10.1111/j.1600-0447.1988.tb05116.x. PMID 2899377.
- ^ a b c d Moncrieff, J. (2006). “Why is it so difficult to stop psychiatric drug treatment? It may be nothing to do with the original problem”. Med Hypotheses 67 (3): 517–23. doi:10.1016/j.mehy.2006.03.009. PMID 16632226.
- ^ Glazer, WM. (2000). “Expected incidence of tardive dyskinesia associated with atypical antipsychotics”. J Clin Psychiatry 61 Suppl 4: 21–6. PMID 10739327.
- ^ Samaha A-N, Seeman P, Stewart J, Rajabi H, Kapur S (2007). “"Breakthrough" Dopamine Supersensitivity during Ongoing Antipsychotic Treatment Leads to Treatment Failure over Time”. The Journal of Neuroscience 27 (11): 2979–2986. doi:10.1523/JNEUROSCI.5416-06.2007. PMID 17360921.
- ^ Gitlin, Michael; Nuechterlein, Keith; Subotnik, Kenneth L.; Ventura, Joseph; Mintz, Jim; Fogelson, David L.; Bartzokis, George; Aravagiri, Manickam (2001). “Clinical Outcome Following Neuroleptic Discontinuation in Patients With Remitted Recent-Onset Schizophrenia”. American Journal of Psychiatry 158 (11): 1835–1842. doi:10.1176/appi.ajp.158.11.1835. ISSN 0002-953X.
- ^ Lambert, TJ. (2007). “Switching antipsychotic therapy: what to expect and clinical strategies for improving therapeutic outcomes”. J Clin Psychiatry 68 Suppl 6: 10–3. PMID 17650054.
- ^ “Medical Term: cross-taper”. Drugs.com. 2013年4月10日閲覧。
- ^ Group, BMJ, ed. (2009-03), “4.2.1”, British National Formulary (57 ed.), United Kingdom: 王立薬剤師会, p. 192, ISBN 978-0853698456, "Withdrawal of antipsychotic drugs after long-term therapy should always be gradual and closely monitored to avoid the risk of acute withdrawal syndromes or rapid relapse."
- ^ Antipsychotics en:David Healy (psychiatrist) - 2016年12月14日閲覧
- ^ 姫井昭男『精神科の薬がわかる本』(1版)医学書院、2008年、113頁。ISBN 978-4-260-00763-4。
- ^ 笠陽一郎『精神科セカンドオピニオン―正しい診断と処方を求めて』シーニュ、2008年7月、204-206頁。ISBN 978-4-9903014-1-5。
- ^ 山田武史 著「12 抗コリン性抗パーキンソン薬について教えて下さい。抗コリン性パーキンソン病を併用することによるデメリットはどのようなものがあるでしょうか?本当に認知機能に影響するのでしょうか?」、藤井康男(編集)、稲垣中(編集協力) 編『統合失調症の薬物療法100のQ&A』星和書店、2008年5月、35-37頁。ISBN 978-4791106677。
- ^ 精神医学講座担当者会議、佐藤光源、丹羽真一、井上新平『統合失調症治療ガイドライン』(2版)医学書院、2008年、133頁。ISBN 978-4-260-00646-0。
- ^ “Practice Guideline for the Treatment of Patients With Schizophrenia Second Edition”. The American Journal of Psychiatry 1 (2 Suppl): 1–56. (February 2006). doi:10.1176/appi.books.9780890423363.45859. PMID 15000267.[リンク切れ]
- ^ Adams, C. E. (2004). “Schizophrenia. Full National Clinical Guideline on Core Interventions in Primary and Secondary Care National Collaborating Centre for Mental Health”. Psychiatric Bulletin 28 (9): 351–351. doi:10.1192/pb.28.9.351. ISSN 0955-6036.
- ^ Leucht, S; Arbter, D; Engel, R R; Kissling, W; Davis, J M (April 2008). “How effective are second-generation antipsychotic drugs? A meta-analysis of placebo-controlled trials”. Molecular Psychiatry 14 (4): 429–447. doi:10.1038/sj.mp.4002136. PMID 18180760.
- ^ Rattehalli, Ranganath D; Jayaram, Mahesh B; Smith, Michael; Rattehalli, Ranganath D (2010). Risperidone versus placebo for schizophrenia. doi:10.1002/14651858.CD006918.pub2.
- ^ Cipriani A, Rendell JM, Geddes J (2009). Cipriani, Andrea. ed. “Olanzapine in long-term treatment for bipolar disorder”. Cochrane Database of Systematic Reviews (Online) (1): CD004367. doi:10.1002/14651858.CD004367.pub2. PMID 19160237.
- ^ a b Hay, Phillipa J.; Spielmans, Glen I.; Berman, Margit I.; Linardatos, Eftihia; Rosenlicht, Nicholas Z.; Perry, Angela; Tsai, Alexander C. (2013). “Adjunctive Atypical Antipsychotic Treatment for Major Depressive Disorder: A Meta-Analysis of Depression, Quality of Life, and Safety Outcomes”. PLoS Medicine 10 (3): e1001403. doi:10.1371/journal.pmed.1001403.
- ^ Patrick V, Levin E, Schleifer S (July 2005). “Antipsychotic polypharmacy: is there evidence for its use?”. Journal of Psychiatric Practice 11 (4): 248–57. doi:10.1097/00131746-200507000-00005. PMID 16041235.
- ^ Ito H, Koyama A, Higuchi T (September 2005). “Polypharmacy and excessive dosing: psychiatrists' perceptions of antipsychotic drug prescription”. The British Journal of Psychiatry 187 (3): 243–7. doi:10.1192/bjp.187.3.243. PMID 16135861.
- ^ a b Grunder, G.; Fellows, C.; Janouschek, H.; Veselinovic, T.; Boy, C.; Brocheler, A.; Kirschbaum, K. M.; Hellmann, S. et al. (August 2008). “Brain and Plasma Pharmacokinetics of Aripiprazole in Patients With Schizophrenia: An [18FFallypride PET Study”]. American Journal of Psychiatry 165 (8): 988–995. doi:10.1176/appi.ajp.2008.07101574. PMID 18381901.
- ^ Ezewuzie, N. (January 2005). “Establishing a dose-response relationship for oral risperidone in relapsed schizophrenia”. Journal of Psychopharmacology 20 (1): 86–90. doi:10.1177/0269881105057001. PMID 16174679.
- ^ Sparshatt, Anna; Jones, Sarah; Taylor, David (2008). “Quetiapine: dose-response relationship in schizophrenia”. CNS Drugs 22 (1): 49–68. doi:10.2165/00023210-200822010-00004. PMID 18072814.
- ^ Kinon, Bruce J.; Volavka, Jan; Stauffer, Virginia; Edwards, Sara E.; et al (August 2008). “Standard and Higher Dose of Olanzapine in Patients With Schizophrenia or Schizoaffective Disorder”. Journal of Clinical Psychopharmacology 28 (4): 392–400. doi:10.1097/JCP.0b013e31817e63a5. PMID 18626265.
- ^ Evidence Lacking to Support Many Off-label Uses of Atypical Antipsychotics (2007). Ahrq.gov.
- ^ James, A.C. (2010). “Prescribing antipsychotics for children and adolescents”. Advances in Psychiatric Treatment 16: 63. doi:10.1192/apt.bp.108.005652.
- ^ Romeo R, Knapp M, Tyrer P, Crawford M, Oliver-Africano P (July 2009). “The treatment of challenging behaviour in intellectual disabilities: cost-effectiveness analysis”. Journal of Intellectual Disability Research 53 (7): 633–43. doi:10.1111/j.1365-2788.2009.01180.x. PMID 19460067.
- ^ Clive G Ballard , Jonathan Waite, Jacqueline Birks (2008年10月8日). “Atypical antipsychotics for aggression and psychosis in Alzheimer's disease” (Abstract). The Cochrane Collaboration.. John Wiley & Sons, Ltd.. 2012年7月27日閲覧。
- ^ “NCT00245206 Side Effects of Newer Antipsychotics in Older Adults (NCT00245206)”. ClinicalTrials.gov. 2013年3月24日閲覧。
- ^ Jin, Hua; Shih, Pei-an Betty; Golshan, Shahrokh; Mudaliar, Sunder; Henry, Robert; Glorioso, Danielle K.; Arndt, Stephan; Kraemer, Helena C. et al. (January 2013). “Comparison of Longer-Term Safety and Effectiveness of 4 Atypical Antipsychotics in Patients Over Age 40”. The Journal of Clinical Psychiatry 74 (01): 10–18. doi:10.4088/JCP.12m08001. PMID 23218100.
- ^ Jablensky A, Sartorius N, Ernberg G, Anker M, Korten A, Cooper J, Day R, Bertelsen A (1992). “Schizophrenia: manifestations, incidence and course in different cultures. A World Health Organization ten-country study”. Psychol Med Monogr Suppl 20: 1–97. doi:10.1017/S0264180100000904. PMID 1565705.
- ^ Hopper K, Wanderling J (2000). “Revisiting the developed versus developing country distinction in course and outcome in schizophrenia: results from ISoS, the WHO collaborative followup project. International Study of Schizophrenia”. Schizophrenia Bulletin 26 (4): 835–46. doi:10.1093/oxfordjournals.schbul.a033498. PMID 11087016.
- ^ Moncrieff J (July 2006). “Does antipsychotic withdrawal provoke psychosis? Review of the literature on rapid onset psychosis (supersensitivity psychosis) and withdrawal-related relapse”. Acta Psychiatrica Scandinavica 114 (1): 3–13. doi:10.1111/j.1600-0447.2006.00787.x. PMID 16774655.
- ^ Harrow M; Jobe TH (May 2007). "Factors involved in outcome and recovery in schizophrenia patients not on antipsychotic medications: a 15-year multifollow-up study". The Journal of Nervous and Mental Disease (英語). 195 (5): 406–414. doi:10.1097/01.nmd.0000253783.32338.6e (inactive 17 March 2010). PMID 17502806。
- ^ Whitaker R (2004). “The case against antipsychotic drugs: a 50-year record of doing more harm than good”. Medical Hypotheses 62 (1): 5–13. doi:10.1016/S0306-9877(03)00293-7. PMID 14728997.
- ^ a b Adam James (2008年3月2日). “Myth of the antipsychotic”. The Guardian. Guardian News and Media Limited. 2012年7月27日閲覧。
- ^ Leucht, S.; Heres, S.; Hamann, J.; Kane, J. M. (March 2008). “Methodological Issues in Current Antipsychotic Drug Trials”. Schizophrenia Bulletin 34 (2): 275–285. doi:10.1093/schbul/sbm159. PMC 2632403. PMID 18234700.
- ^ トーマス・インセル (2013年8月28日). “Antipsychotics: Taking the Long View”. NIMH Director’s Blog. 2014年2月26日閲覧。
- ^ a b c Insel TR (April 2009). “Disruptive insights in psychiatry: transforming a clinical discipline”. J. Clin. Invest. 119 (4): 700–5. doi:10.1172/JCI38832. PMC 2662575. PMID 19339761 2013年1月7日閲覧。.
- ^ a b Peluso, M. J.; Lewis, S. W.; Barnes, T. R. E.; Jones, P. B. (May 2012). “Extrapyramidal motor side-effects of first- and second-generation antipsychotic drugs”. The British Journal of Psychiatry 200 (5): 387–392. doi:10.1192/bjp.bp.111.101485. PMID 22442101.
- ^ a b Miller DD, Caroff SN, Davis SM, et al. (October 2008). “Extrapyramidal side-effects of antipsychotics in a randomised trial”. Br J Psychiatry 193 (4): 279–88. doi:10.1192/bjp.bp.108.050088. PMC 2801816. PMID 18827289.
- ^ Ito, Hiroshi; Arakawa, Ryosuke; Takahashi, Hidehiko; Takano, Harumasa; Okumura, Masaki; Otsuka, Tatsui; Ikoma, Yoko; Shidahara, Miho et al. (June 2008). “No regional difference in dopamine D2 receptor occupancy by the second-generation antipsychotic drug risperidone in humans: a positron emission tomography study”. The International Journal of Neuropsychopharmacology 12 (05): 667. doi:10.1017/S1461145708009577. PMID 18937879.
- ^ Geddes J, Freemantle N, Harrison P, Bebbington P (December 2000). “Atypical antipsychotics in the treatment of schizophrenia: systematic overview and meta-regression analysis”. BMJ 321 (7273): 1371–6. doi:10.1136/bmj.321.7273.1371. PMC 27538. PMID 11099280.
- ^ a b c d Horacek J, Bubenikova-Valesova V, Kopecek M et al. (2006). “Mechanism of action of atypical antipsychotic drugs and the neurobiology of schizophrenia”. CNS Drugs 20 (5): 389–409. doi:10.2165/00023210-200620050-00004. PMID 16696579.
- ^ Leucht S, Wahlbeck K, Hamann J, Kissling W (May 2003). “New generation antipsychotics versus low-potency conventional antipsychotics: a systematic review and meta-analysis”. Lancet 361 (9369): 1581–9. doi:10.1016/S0140-6736(03)13306-5. PMID 12747876.
- ^ Davis JM, Chen N, Glick ID (June 2003). “A meta-analysis of the efficacy of second-generation antipsychotics”. Archives of General Psychiatry 60 (6): 553–64. doi:10.1001/archpsyc.60.6.553. PMID 12796218.
- ^ Tuunainen A, Wahlbeck K, Gilbody SM (2000). Tuunainen, Arja. ed. “Newer atypical antipsychotic medication versus clozapine for schizophrenia”. Cochrane Database of Systematic Reviews (2): CD000966. doi:10.1002/14651858.CD000966. PMID 10796559.
- ^ Ghaemi SN, Hsu DJ, Rosenquist KJ, Pardo TB, Goodwin FK (March 2006). “Extrapyramidal side effects with atypical neuroleptics in bipolar disorder”. Progress in Neuro-psychopharmacology & Biological Psychiatry 30 (2): 209–13. doi:10.1016/j.pnpbp.2005.10.014. PMID 16412546.
- ^ Lieberman JA, Stroup TS, McEvoy JP et al. (September 2005). “Effectiveness of antipsychotic drugs in patients with chronic schizophrenia”. The New England Journal of Medicine 353 (12): 1209–23. doi:10.1056/NEJMoa051688. PMID 16172203.
- ^ Meltzer and Bobo (2006) "Interpreting the Efficacy Findings in the CATIE Study: What Clinicians Should Know" CNS Spectr.11(7 Suppl 7):14-24
- ^ Leucht, Stefan; Corves, Caroline; Arbter, Dieter; Engel, Rolf R; Li, Chunbo; Davis, John M (January 2009). “Second-generation versus first-generation antipsychotic drugs for schizophrenia: a meta-analysis”. The Lancet 373 (9657): 31–41. doi:10.1016/S0140-6736(08)61764-X. PMID 19058842.
- ^ Stroup T; Lieberman, JA; McEvoy, JP; Swartz, MS; Davis, SM; Rosenheck, RA; Perkins, DO; Keefe, RS et al. (2006). “Effectiveness of olanzapine, quetiapine, risperidone, and ziprasidone in patients with chronic schizophrenia following discontinuation of a previous atypical antipsychotic”. Am J Psychiatry 163 (4): 611–22. doi:10.1176/appi.ajp.163.4.611. PMID 16585435.
- ^ McEvoy J; Lieberman, JA; Stroup, TS; Davis, SM; Meltzer, HY; Rosenheck, RA; Swartz, MS; Perkins, DO et al. (2006). “Effectiveness of clozapine versus olanzapine, quetiapine, and risperidone in patients with chronic schizophrenia that did not respond to prior atypical antipsychotic treatment”. Am J Psychiatry 163 (4): 600–10. doi:10.1176/appi.ajp.163.4.600. PMID 16585434.
- ^ Voruganti LP, Baker LK, Awad AG (March 2008). “New generation antipsychotic drugs and compliance behaviour”. Current Opinion in Psychiatry 21 (2): 133–9. doi:10.1097/YCO.0b013e3282f52851. PMID 18332660.
- ^ Owens, D. C. (2008). “How CATIE brought us back to Kansas: a critical re-evaluation of the concept of atypical antipsychotics and their place in the treatment of schizophrenia”. Advances in Psychiatric Treatment 14 (1): 17–28. doi:10.1192/apt.bp.107.003970.
- ^ Typical and Atypical Antipsychotics - The Misleading Dichotomy (2008). Content.karger.com.
- ^ Casey, D (March 1999). “Tardive dyskinesia and atypical antipsychotic drugs”. Schizophrenia Research 35: S61–S66. doi:10.1016/S0920-9964(98)00160-1. PMID 10190226.
- ^ 英国国立医療技術評価機構 2014, Chapt.1.3.5.
- ^ Lieberman JA, Stroup TS, McEvoy JP, et al. (September 2005). “Effectiveness of antipsychotic drugs in patients with chronic schizophrenia”. N. Engl. J. Med. 353 (12): 1209–23. doi:10.1056/NEJMoa051688. PMID 16172203.
- ^ a b Findling RL, Johnson JL, McClellan J, et al. (June 2010). “Double-blind maintenance safety and effectiveness findings from the Treatment of Early-Onset Schizophrenia Spectrum (TEOSS) study”. J Am Acad Child Adolesc Psychiatry 49 (6): 583–94; quiz 632. doi:10.1016/j.jaac.2010.03.013. PMC 2882800. PMID 20494268.
- ^ Makhinson, Michael (January 2010). “Biases in Medication Prescribing: The Case of Second-Generation Antipsychotics”. Journal of Psychiatric Practice 16 (1): 15–21. doi:10.1097/01.pra.0000367774.11260.e4. PMID 20098227.
- ^ Leucht S, Cipriani A, Spineli L, Mavridis D, Orey D, Richter F, Samara M, Barbui C, Engel RR, Geddes JR, Kissling W, Stapf MP, Lässig B, Salanti G, Davis JM (2013-09-14). “Comparative efficacy and tolerability of 15 antipsychotic drugs in schizophrenia: a multiple-treatments meta-analysis”. en:The Lancet 382 (9896): 951-62. doi:10.1016/S0140-6736(13)60733-3. PMID 23810019.
- ^ a b Sogawa R, Shimomura Y, Minami C, Maruo J, Kunitake Y, Mizoguchi Y, Kawashima T, Monji A, Hara H. (2016-8). “Aripiprazole-Associated Hypoprolactinemia in the Clinical Setting.”. en:Journal of Clinical Psychopharmacology. 36 (4): 385-7. doi:10.1097/JCP.0000000000000527. PMID 27281387.
- ^ FDA Drug Safety Communication: FDA warns about new impulse-control problems associated with mental health drug aripiprazole (Abilify, Abilify Maintena, Aristada) (05-03-2016 FDA)
- ^ Moore TJ, Glenmullen J, Furberg CD. (2010-12-15). “Prescription drugs associated with reports of violence towards others.”. PLoS One. 5 (12): e15337. doi:10.1371/journal.pone.0015337. PMC 3002271. PMID 21179515.
- ^ Seeman P, Ko F, Tallerico T. (2005-9). “Dopamine receptor contribution to the action of PCP, LSD and ketamine psychotomimetics.”. en:Molecular Psychiatry. 10 (9): 877-83. doi:10.1038/sj.mp.4001682. PMID 15852061.
- ^ Seeman P, Guan HC, Hirbec H. (2009-8). “Dopamine D2High receptors stimulated by phencyclidines, lysergic acid diethylamide, salvinorin A, and modafinil.”. en:Synapse. 63 (8): 698-704. doi:10.1002/syn.20647. PMID 19391150.
- ^ Ilyin, VI; Whittemore, ER; Guastella, J; Weber, E; Woodward, RM (1996). “Subtype-selective inhibition of N-methyl-D-aspartate receptors by haloperidol”. en:Molecular Pharmacology 50 (6): 1541-50. PMID 8967976.
- ^ a b エリオット・S・ヴァレンスタイン 2008, pp. 27–28.
- ^ デイヴィッド・ヒーリー 2012, p. 113.
- ^ a b デイヴィッド・ヒーリー 2012, p. 223-225.
- ^ Miller, G. (July 2010). “Is Pharma Running Out of Brainy Ideas?” (pdf). Science 329 (5991): 502–504. doi:10.1126/science.329.5991.502. PMID 20671165.
- ^ a b Pipeline antipsychotic drugs to drive next market evolution (2009). Healthcarefinancenews.com (7 August 2009).
- ^ Aparasu, R. R.; Bhatara, V. (December 2006). “Antipsychotic Use and Expenditure in the United States”. Psychiatric Services 57 (12): 1693–1693. doi:10.1176/appi.ps.57.12.1693. PMID 17158480.
- ^ 2008 U.S. Sales and Prescription Information: Top Therapeutic Classes by U.S. Sales (PDF). Imshealth.com.
- ^ GPs under 'pressure' to issue neuroleptics, claims professor, Chemist + Druggist, 15 January 2009
- ^ Nick Triggle (2009年11月12日). “Dementia drug use 'killing many'”. BBC 2013年5月7日閲覧。
- ^ “UK study warns against anti-psychotics for dementia”. reuters. (2009年11月12日) 2013年5月7日閲覧。
- ^ Hilzenrath, David S. (2010年1月16日). “Justice suit accuses Johnson & Johnson of paying kickbacks”. The Washington Post 2010年1月17日閲覧。
- ^ a b Jobe TH, Harrow M (December 2005). “Long-term outcome of patients with schizophrenia: a review” (PDF). Canadian Journal of Psychiatry 50 (14): 892–900. PMID 16494258. オリジナルの2011年7月25日時点におけるアーカイブ。 2008年7月5日閲覧。.
- ^ Kane, JM.; Leucht, S. (Mar 2008). “Unanswered Questions in Schizophrenia Clinical Trials”. Schizophr Bull 34 (2): 302–9. doi:10.1093/schbul/sbm143. PMC 2632396. PMID 18199633.
- ^ a b c Wilson, Duff (2010年10月2日). “Side Effects May Include Lawsuits”. New York Times. 2012年1月5日閲覧。
- ^ DUFF WILSON (2009年2月27日). “Drug Maker’s E-Mail Released in Seroquel Lawsuit”. The New York Times. The New York Times Company. 2012年7月27日閲覧。
- ^ Gosden R, Beder S (2001). “Pharmaceutical industry agenda setting in mental health policies”. Ethical Human Sciences and Services : an International Journal of Critical Inquiry 3 (3): 147–59. PMID 15278977.
- ^ Alex Berenson (2007年1月4日). “Lilly to Pay Up to $500 Million to Settle Claims”. The New York Times 2013年3月15日閲覧。
- ^ a b c Robert Whitaker 2009, pp. 355–357 (翻訳書は ロバート・ウィタカー 2010, pp. 528–531)
- ^ a b Peter C. Gøtzsche 2015, § Forced treatment must be banned
- ^ a b “Supreme Court of Alaska. No. S-11021.”. Thomson Reuters (2006年6月30日). 2018年7月2日閲覧。
- ^ a b “Alaska Forced Medication Case”. Law Project for Psychiatric Rights. 2018年7月2日閲覧。
- ^ “#07-782: 09-28-07 Bristol-Myers Squibb to Pay More Than $515 Million to Resolve Allegations of Illegal Drug Marketing and Pricing”. Justice.gov (2007年9月28日). 2012年11月30日閲覧。
- ^ “Pharmaceutical Company Eli Lilly to Pay Record $1.415 Billion for Off-Label Drug Marketing” (pdf). Justice.gov (2009年1月15日). 2012年10月17日時点のオリジナルよりアーカイブ。2013年2月23日閲覧。
- ^ “Pharmaceutical Company Pfizer, Inc. To Pay $301 Million for Off-Label Drug Marketing”. Justice.gov (2009年9月2日). 2013年2月23日閲覧。
- ^ “Pharmaceutical Giant AstraZeneca to Pay $520 Million for Off-label Drug Marketing”. Justice.gov (2010年4月27日). 2012年11月30日閲覧。
- ^ Michael Muskal (2012年4月11日). “Companies belittled risks of Risperdal, slapped with huge fine”. Los Angels Times 2013年2月23日閲覧。
- ^ Rohleder, Cathrin; Müller, Juliane K.; Lange, Bettina; et al. (2016). “Cannabidiol as a Potential New Type of an Antipsychotic. A Critical Review of the Evidence”. Frontiers in Pharmacology 7: 422. doi:10.3389/fphar.2016.00422. PMC 5099166. PMID 27877130.
- ^ World Health Organization; 日本臨床カンナビノイド学会 (6 December 2017). カンナビジオール(CBD)事前審査報告書 (pdf) (Report). 世界保健機関. p. 18. 2017年12月5日閲覧。 日本臨床カンナビノイド学会 World Health Organization (6 December 2017). CANNABIDIOL Pre-Review Report Agenda Item 5.2 : Expert Committee on Drug Dependence Thirty-ninth Meeting (pdf) (Report). 世界保健機関. 2017年12月5日閲覧。
- ^ a b Guinguis R, Ruiz MI, Rada G (2017-08-09). “Is cannabidiol an effective treatment for schizophrenia?”. Medwave. 17 (7): e7010. doi:10.5867/medwave.2017.07.7010. PMID 28820868.
- ^ McGuire, Philip; Robson, Philip; Cubala, Wieslaw Jerzy; et al. (2017). “Cannabidiol (CBD) as an Adjunctive Therapy in Schizophrenia: A Multicenter Randomized Controlled Trial”. American Journal of Psychiatry: appi.ajp.2017.1. doi:10.1176/appi.ajp.2017.17030325. PMID 29241357.
- ^ Pawełczyk, Tomasz; Grancow, Marta; Kotlicka-Antczak, Magdalena; et al. (2015). “Omega-3 fatty acids in first-episode schizophrenia - a randomized controlled study of efficacy and relapse prevention (OFFER): rationale, design, and methods”. BMC Psychiatry 15 (1): 97. doi:10.1186/s12888-015-0473-2. PMC 4456694. PMID 25934131.
- ^ “Microglia and Brain Plasticity in Acute Psychosis and Schizophrenia Illness Course: A Meta-Review”. Front Psychiatry 8: 238. (2017-11-16). doi:10.3389/fpsyt.2017.00238. PMC 5696326. PMID 29201010.
- ^ “Increased microglial synapse elimination in patient-specific models of schizophrenia”. BioRxiv. (2017-12-8). doi:10.1101/231290.
- ^ 厚生労働省健康局結核感染症課 (June 2017). 抗微生物薬適正使用の手引き 第一版 (pdf) (Report). 厚生労働省. 2017年12月10日閲覧。
参考文献
[編集]診療ガイドライン
- 『mhGAP Intervention Guide for mental, neurological and substance use disorders in non-specialized health settings(リンク切れ)』(レポート)世界保健機関、2010年。ISBN 9789241548069。
- CG178: Psychosis and schizophrenia in adults: treatment and management (Report). 英国国立医療技術評価機構. 12 February 2014.
- CG185: Bipolar disorder: the assessment and management of bipolar disorder in adults, children and young people in primary and secondary care (Report). 英国国立医療技術評価機構. 24 September 2014.
それ以外
- エリオット・S・ヴァレンスタイン 著、功刀浩監訳、中塚公子 訳『精神疾患は脳の病気か?』みすず書房、2008年2月。ISBN 978-4-622-07361-1。、Blaming the Brain, 1998
- デイヴィッド・ヒーリー 著、江口重幸監訳、坂本響子 訳『双極性障害の時代―マニーからバイポーラーへ』みすず書房、2012年11月。ISBN 978-4-622-07720-6。、MANIA: A Short History of Bipolar Disorder, 2008
- Robert Whitaker (2009-01-01), Anatomy of an Epidemic: Magic Bullets, Psychiatric Drugs, and the Astonishing Rise of Mental Illness in America, New York: Crown Publishing Group, ASIN B004RU7U5C.(翻訳書は ロバート・ウィタカー『心の病の「流行」と精神科治療薬の真実』小野善郎監訳、門脇陽子・森田由美訳、福村出版、2010年9月19日。ISBN 978-4571500091。)
- Peter C. Gøtzsche (2015-09-01), Deadly Psychiatry and Organised Denial, ArtPeople, ASIN B014SO7GHS.