Kupfer(II)-sulfid
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| _ Cu2+ _ S2− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kupfer(II)-sulfid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Verhältnisformel | CuS | ||||||||||||||||||
| Kurzbeschreibung |
schwarzer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 95,61 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser (0,33 mg l−1, 18 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
0,1 mg·m−3 [1] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Kupfer(II)-sulfid ist eine chemische Verbindung des Kupfers und Schwefels. Es ist ein schwarzer, spröder Feststoff mit der Verhältnisformel CuS. Trotz dieser Verhältnisformel liegen in der Verbindung nicht nur Cu2+-Ionen vor, sondern sie besteht aus einer Mischung von Cu+- und Cu2+-Ionen sowie Sulfidionen und Disulfidionen. Das genaue Verhältnis ist Cu2ICuII(S2)S.[3]
Vorkommen
[Bearbeiten | Quelltext bearbeiten]In der Natur kommt Kupfer(II)-sulfid als das Mineral Covellin vor.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Kupfer(II)-sulfid wird (im Labor) durch Fällung aus wässriger Lösung dargestellt, beispielsweise durch Einleiten von Schwefelwasserstoff.[4]
Beim so hergestellten Kupfersulfid handelt es sich um Covellin.[3]
Hochreines Kupfer(II)-sulfid erhält man durch Reaktion einer Kupfer(I)-sulfid/Schwefel-Mischung bei Raumtemperatur.[4]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Kupfer(II)-sulfid ist ein schwarzer, wasserunlöslicher Feststoff, der in der Natur als sulfidisches Kupfererz vorkommt. Er ist elektrisch leitfähig.
In feuchter Luft wird das Erz Kupfer(II)-sulfid zu Kupfersulfat oxidiert. In trockener Luft bei Raumtemperatur ist die Verbindung stabil. Wird Kupfer(II)-sulfid unter Luftausschluss erhitzt, zerfällt es bei 507 °C zu Kupfer(I)-sulfid und Schwefel. Das entstandene Kupfersulfid ist aber nicht stöchiometrisch aufgebaut und lässt sich durch die Form Cu2-xS besser beschreiben.[2]
Das Rösten des Erzes an Luft führt hingegen zu Kupfer(II)-oxid und Schwefeldioxid.
Physikalische Eigenschaften
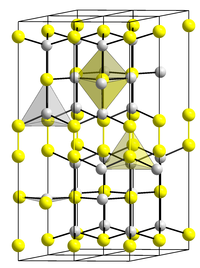
[Bearbeiten | Quelltext bearbeiten]Kupfer(II)-sulfid hat eine hexagonale Kristallstruktur mit der Raumgruppe P63/mmc (Raumgruppen-Nr. 194) (a = 3,794 Å, c = 16,33 Å) und eine Bildungsenthalpie von −48,5 kJ/mol.[4] Die Elementarzelle besteht aus 6 Formeleinheiten. 4 Cu+-Kationen sind tetraedrisch von S2--Anionen umgeben, die 2 übrigen Cu2+-Kationen sind trigonal planar von S22--Hanteln umgeben. 4 der 6 Schwefelatome bilden Hanteln mit einem Abstand von 207,1 pm, woraus auf S22--Anionen geschlossen werden kann. Die übrigen zwei S2--Anionen umgeben die trigonal planar koordinierten Kupferzentren, während sie selbst von 5 Kupferatomen in Form einer trigonalen Bipyramide koordiniert werden. Die Disulfidanionen werden tetraedrisch von Kupfer umgeben.[5][6] Aus diesen Erkenntnissen ergibt sich korrekte Summenformel Cu2ICuII(S2)S und die Bezeichnung Kupfer(I,II)-sulfid.[3]
 |
 |
 |

| |
| Stäbchenmodell von Covellin | trigonal planare Koordination des Kupfers |
tetraedrische Koordination des Kupfers |
trigonal bipyramidale Koordination des Schwefels |
tetraedrische Koordination der Disulfideinheit |
Bei etwa 100 °C kommt es zum Phasenübergang zum monoklinen Kristallsystem.[7]
Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Kupfer(II)-sulfid ist löslich nur in konzentrierten, oxidierenden Säuren. In verdünnten Säuren ist es unlöslich. Im Kationentrenngang wird es daher schon bei pH 4–5 in der Schwefelwasserstoffgruppe ausgefällt, in Salpetersäure gelöst und mit Ammoniakwasser als Kupfertetramminkomplex nachgewiesen (Nachweise für Kationen, Nachweisreaktion).
Verwendung
[Bearbeiten | Quelltext bearbeiten]Kupfer(II)-sulfid wird für fäulnishemmende Anstriche verwendet.
In den 1970er und 1980er Jahren wurde Kupfer(II)-sulfid als eher seltenes Kathodenmaterial in Lithium-Batterien verwendet.[8] Die Firma Duracell stellte Flachzellen für Herzschrittmacher mit CuS her.[9]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Eintrag zu Kupfer(II)-sulfid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 19. Dezember 2019. (JavaScript erforderlich)
- ↑ a b R. Blachnik, A. Müller: The formation of Cu2S from the elements. I. Copper used in form of powders. In: Thermochimica Acta. Band 361, Nr. 1–2, Oktober 2000, S. 31–52, doi:10.1016/S0040-6031(00)00545-1.
- ↑ a b c A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ a b c Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 982.
- ↑ Ivar Oftedal: Die Kristallstruktur des Covellins (CuS). In: Zeitschrift für Kristallographie - Crystalline Materials. Band 83, Nr. 1-6, 1932, S. 9–25, doi:10.1524/zkri.1932.83.1.9.
- ↑ Howard T. Evans, Judith A. Konnert: Crystal structure refinement of covellite. In: American Mineralogist. Band 61, 1976, S. 996–1000 (englisch, minsocam.org [PDF; 577 kB; abgerufen am 13. Oktober 2019]).
- ↑ LK-99 isn’t a superconductor — how science sleuths solved the mystery Replications pieced together the puzzle of why the material displayed superconducting-like behaviours.
- ↑ S. C. Levy, P. Bro: Battery Hazards and Accident Prevention. Springer, 1994, ISBN 978-0-306-44758-7 (google.com).
- ↑ https://www.google.de/books/edition/Proceedings_of_the_Symposium_on_Lithium/LuWyAAAAIAAJ?hl=en&gbpv=1&pg=PA23&printsec=frontcover




