Глицерин
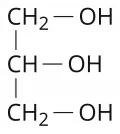
Глицери́н (от греч. γλυκερός – сладкий), глицерол, 1,2,3-пропантриол, пропан-1,2,3-триол, 1,2,3-триоксипропан, CH2OHCHOHCH2OH, органическое соединение, трёхатомный спирт. Молярная масса 92,09 г/моль, плотность 1,2604 г/см3, показатель преломления 1,4729, температура плавления 20 °C, температура кипения 290 °C (с разложением). Глицерин первые был получен К. В. Шееле в 1779 г. при омылении жиров.
Физико-химические свойства
Глицерин – вязкая жидкость без цвета и запаха, обладает сладковатым вкусом, в любых пропорциях смешивается с водой, этанолом, мало растворима в диэтиловом эфире, нерастворима в бензоле, хлороформе, четырёххлористом углероде, сероуглероде, петролейном эфире.
При смешивании глицерина с водой выделяется тепло и происходит контракция (уменьшение объёма); растворы глицерина с водой замерзают при низких температурах (например, для раствора, содержащего 66,7 % глицерина, tпл= –46,5 °С).
Безводный глицерин обладает высокой гигроскопичностью – хорошо поглощает влагу из воздуха (до 40 % по массе).
Глицерин растворяет многие органические и неорганические соединения (например, йод, бром, фенол, тимол, хлорид ртути, алкалоиды).
Глицерин является слабой кислотой (рКа=13,9), взаимодействует со щелочными металлами с образованием моно-, ди- и триглицератов. С аналитической точки зрения интересно образование хелатных солей меди (II), имеющих глубокую синюю окраску.
Взаимодействие с алкилгалогенидами, алкилсульфатами, алкилсульфонатами приводит к О-алкилированию глицерина. Под действием неорганических и органических кислот и их функциональных производных происходит О-ацилирование глицерина. Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов. Окисление глицерина даёт смесь соответствующего альдегида и кетона. При дегидратации глицерина отщепляются две молекулы воды и образуется ненасыщенный альдегид – акриловый.
Способы получения
Основной путь получения глицерина – омыление жиров (глицерин выделяется как побочный продукт).
Синтетически глицерин можно получить из пропена: хлорированием или окислением в акролеин, восстановлением последнего до аллилового спирта с последующим гидроксилированием. Возможно также получение глицерина за счёт каталитического гидрирования глюкозы (восстановление альдегидной группы с одновременным разрывом С3-С4 связи).
Участие в обмене веществ
Глицерин – структурный элемент жиров (триацилглицеролов), служащих поставщиком энергии, и большинства фосфолипидов – основного компонента клеточных мембран. После расщепления жиров глицерин с током крови поступает в печень, где используется для синтеза глюкозы.
Применение
Глицерин как увлажняющее средство и как растворитель используют в фармацевтике, медицине и косметологии. В пищевой промышленности глицерин применяют как эмульгатор, влагоудерживающее вещество, загуститель, разделяющий агент (пищевая добавка Е422). Кроме того, глицерин используют в производстве пластмасс, в сельском хозяйстве, в текстильной, бумажной, лакокрасочной и кожевенной отраслях промышленности. Значительное количество глицерина расходуется на получение тринитрата глицерина (нитроглицерина), на основе которого производят одно из самых известных взрывчатых веществ – динамит. Тринитрат глицерина применяют также в медицине в виде спиртового раствора или таблеток.